电位滴定法测定食品中氨基酸的方法介绍
氨基酸的测定——电位滴定法
1、原理
氨基酸具有酸性基团—COOH和碱性基团—NH2,利用氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,将酸度计的玻璃电极及甘汞电极同时插入被测液中构成电池,用氢氧化钠标准溶液滴定,依据酸度计指示的pH值判断和控制滴定终点。
2、仪器
①酸度计。
②磁力搅拌器。
③微量滴定管(10mL)。
3、试剂
①36%中性甲醛溶液。
②氢氧化钠标准溶液[c(NaOH)=0.0500mol/L]。
4、操作方法
吸取含氨基酸约20mg的试样溶液于10mL容量瓶中,加水定容,混匀后吸取20.0mL,置于200mL烧杯中,加水60mL,插入酸度计的指示电极和参比电极,开动磁力搅拌器,用氢氧化钠标准溶液(0.0500mol/L)滴定至酸度计指示pH=8.2,记录消耗氢氧化钠标准溶液的体积(mL),供计算总酸度含量。
加入10.0mL甲醛溶液,混匀,再用上述氢氧化钠标准溶液继续滴定至pH=8.2,记录消耗氢氧化钠标准溶液的体积(mL)。
同时取80mL蒸馏水置于另一200mL洁净烧杯中,先用氢氧化钠标准溶液滴定至pH=8.2,此时不计标准碱溶液消耗量,再加入10.00mL中性甲醛溶液(36%),用氢氧化钠标准溶液(0.0500mol/L)滴定至pH=8.2,作为试剂空白试验。
5、计算
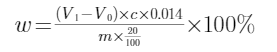
式中 w——试样中氨基酸态氮的质量分数,%;
c——氢氧化钠标准溶液的浓度,mol/L;
V1——滴定至终点(pH=8.2)时消耗氢氧化钠标准溶液的体积,mL;
Vo——空白试验滴定至终点(pH=8.2)时消耗氢氧化钠标准溶液的体积,mL;
m——测定用试样溶液相当于试样的质量,g;
0.014——1mL氢氧化钠标准溶液[c(NaOH)=0.0500mol/L]相当于氮的质量,g。
6、说明及注意事项
①本方法为《酱油卫生标准的分析方法》(GB/T5009.39-1996)中规定的氨基酸态氮的测定方法。本方法准确快速,可适用于各类食品氨基酸态氮含量的测定。
②对于浑浊和色深样液可不经处理而直接测定。
③36%甲醛试剂应避光存放,不含有聚合物(无沉淀)。
④试样中如含有铵盐会影响氨基酸态氮的测定,可使氨基酸态氮测定结果偏高。因此要同时测定铵盐,将氨基酸态氮的结果减去铵盐的结果比较准确。




















