JCI解析: CD8+T细胞的分裂命运受谁调配?
疫苗和癌症免疫疗法在本质上是一样的:它们能够调动免疫系统,使其更好地防御入侵者,例如微生物、恶性肿瘤等。这两种策略都集中于CD8+T细胞。通常在免疫应答过程中,CD8+T细胞会发生不对称分裂,产生两种职责的子细胞——免疫效应T细胞,以杀手的身份消灭入侵者;记忆T细胞,提供长期的保护。
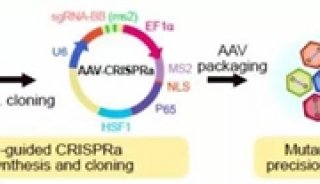
现在,来自于加州大学圣地亚哥医学院的研究人员发现,决定CD8+T细胞分化倾向(记忆细胞和效应细胞)的关键因素是细胞内的蛋白酶体活性。他们证实,激活细胞蛋白酶体的药物能够促使更多的记忆细胞产生。反过来,抑制蛋白酶体会催化更多的效应细胞。
这一方法有望改善疫苗、免疫疗法的作用效果以及延长它们的持续时间。相关研究成果于8月28日发表在《Journal of Clinical Investigation》期刊。
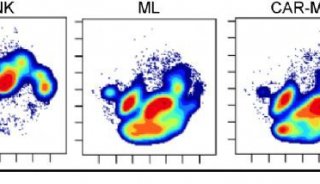
以小鼠和细胞为模型,加州大学圣地亚哥医学院的副教授John T. Chang和团队发现两种不同类型的CD8+T细胞——免疫效应细胞和记忆细胞在蛋白酶体活跃度上有所不同。作为细胞的重要组成部件,蛋白酶体负责降解、回收受损或者不需要的蛋白质。
他们发现,操控蛋白酶体的活性,能够改变细胞的功能!
目前,已有靶向蛋白酶体的药物上市,例如Bortezomib,一种适用于多发性骨髓瘤的抗癌药物,通过抑制蛋白酶体活性而发挥作用。研究团队证实,环孢霉素(cyclosporine),接受器官移植的患者服用的一种免疫抑制药物,能够激活CD8+T细胞中的蛋白酶体。而且,在微生物感染的初期,用环孢霉素处理CD8+T细胞能够促使其产生两倍多的记忆细胞。
“虽然迄今为止,这项工作仅仅在动物和细胞模型上进行了验证,但是我们希望这一方法能够早日被验证用于辅助疫苗和免疫疗法,使其产生更好的免疫防御效果。” John T. Chang教授表示。