阿法替尼治疗EGFR非经典突变晚期肺腺癌经验分享-3
阿法替尼治疗EGFR非经典突变晚期肺腺癌经验分享
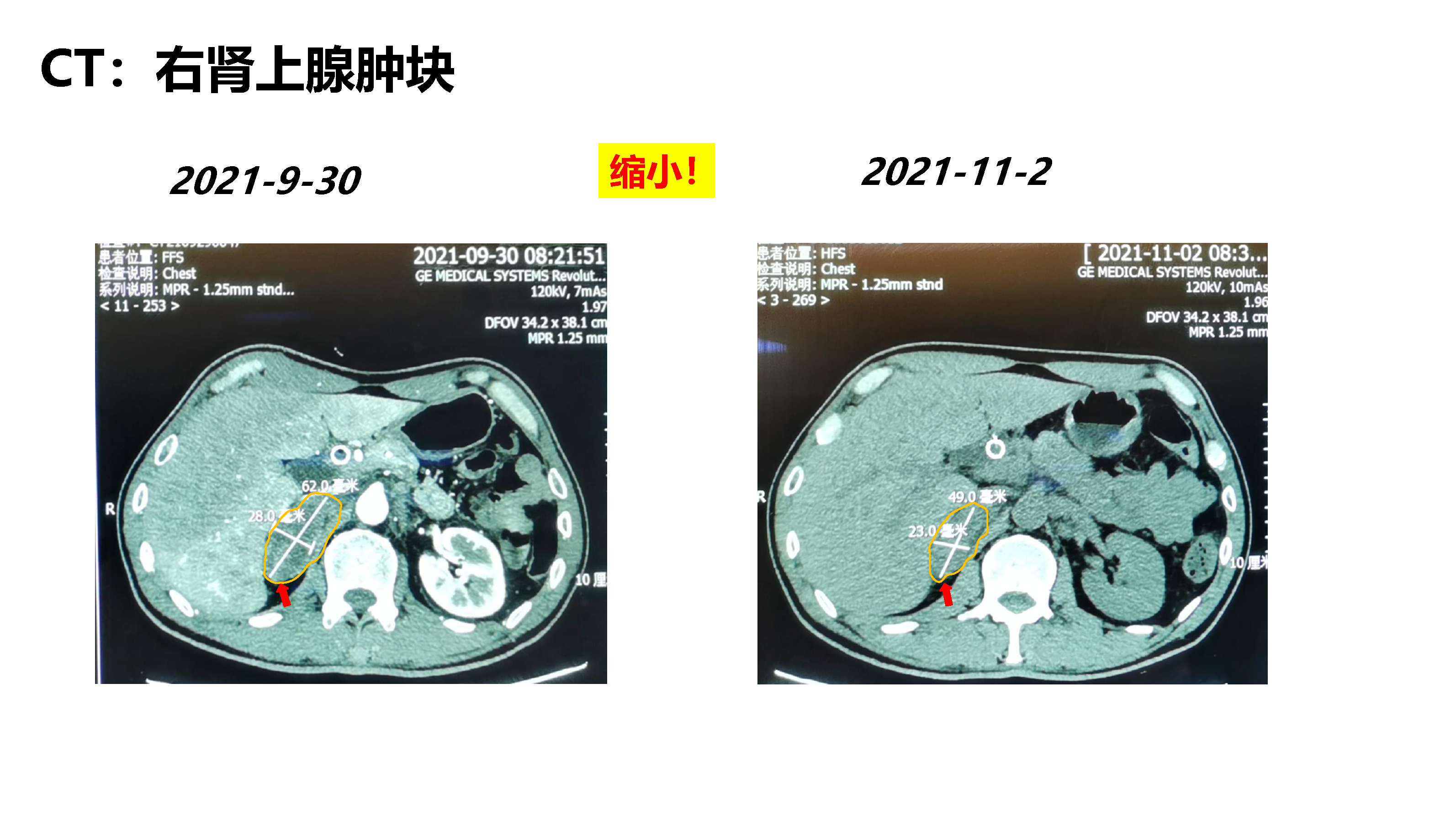



专家点评

EGFR基因突变是非小细胞肺癌(NSCLC)中最常见的突变,欧美人群EGFR突变率约占10%-15%,亚裔人群突变率高达40%-50% [1]。EGFR 19外显子缺失和21外显子L858R点突变统称为经典突变[2],随着分子生物学和二代测序技术的飞速发展,越来越多的EGFR非经典突变类型被发现。EGFR驱动基因最常见的突变位点是Exon 19 第747号到752号氨基酸残基附近的缺失突变,约占45%,其次是Exon21点突变L858R突变,约占35%[3];除此之外被称为非经典突变,约占10%-20%[4-6],其中20外显子插入突变约为13%,19外显子插入突变约为0.2% [2](图1、图2)。

图1:EGFR突变类型
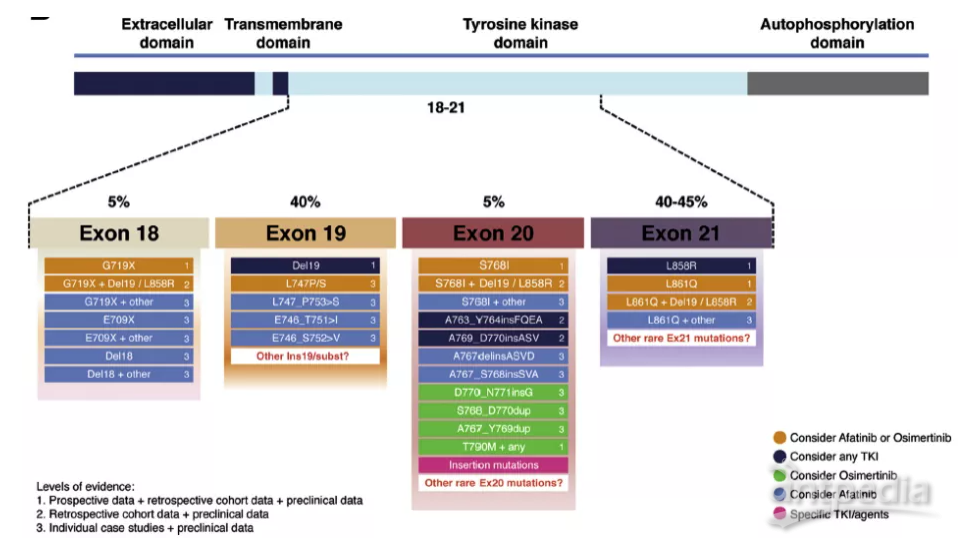
图2:主要非经典突变的EGFR突变患者主要治疗选择推荐
EGFR-TKI三代同堂,到底应该如何选择才能获得最优的疗效和最小的毒副作用,是当今临床研究的热点。近来,有一项头对头前瞻性临床研究证实二代、三代TKI比一代TKI疗效更佳[7],奥希替尼较一代TKI更具生存获益且耐受性良好,对于EGFR经典敏感突变患者,是首选TKI[8]。但是对于EGFR非经典突变患者,如何选择治疗方案,是临床难点。
一代TKI(吉非替尼、厄洛替尼、埃克替尼)药效学机理,都是与过表达或过度活化的EGFR上ATP结合位点可逆地结合,抑制EGFR磷酸化酪氨酸残基的形成。二代TKI(阿法替尼、达克替尼、来那替尼)均为EGFR和ErbB的不可逆抑制剂,除竞争性地占据EGFR上ATP结合位点外,还能与EGFR结合口袋开口处附近特有的氨基酸残基发生烷基化作用或共价键结合,进而实现对EGFR的不可逆抑制。三代TKI(奥希替尼)是单苯胺基嘧啶小分子,丙烯酰胺基与EGFR基因催化域ATP结合位点边缘的C77形成共价结合,从而与特定的EGFR突变形式进行不可逆结合。
除了20外显子插入突变外,主要非经典突变包括Exon18 G719X(G719S、G719A、G719C、G719D)、Exon20 S768I、Exon21 L861Q[9],占比分别为3%、1%、1%[10]。临床前研究发现,EGFR主要非经典突变对二代、三代EGFR-TKI效果要优于一代TKI[10]。
现有的临床研究常会把EGFR罕见突变的患者剔除,所以目前缺乏相关的前瞻性临床证据。LUX-Lung 2/3/6研究的合并分析[11],是迄今为止样本量最大的前瞻性分析。在接受阿法替尼治疗的600例患者中,75例(13%)患者携带非经典EGFR突变,18例携带Exon18 G719X突变,16例携带Exon21 L861Q突变,8例携带Exon20 S768I。使用阿法替尼后疗效显著,客观缓解率(ORR)分别为78%、56%、100%,无进展生存期(PFS)分别为13.8个月、8.2个月、14.7个月,其中有3例患者(G719X、K739_1744dup6以及L858R+Q709G/V各1例)获得完全缓解。基于这项合并分析的结果,美国FDA将阿法替尼适应证扩大至非耐药性EGFR突变的NSCLC患者。
2020年中国台湾的Yang等人利用数据库(https://www.uncommonegfrmutations.com)平台回顾性分析了693例非经典EGFR突变患者使用阿法替尼的数据[9],包括主要非经典突变(Exon18 G719X、Exon20 S768I、Exon21 L861Q)、20外显子插入突变(除外T790M突变)、复合突变、T790M突变阳性、以及其他。随后,在2021年ESMO大会上,研究者再次更新了该数据库中1023例患者的数据,证实阿法替尼一线治疗常见非经典EGFR突变、复合突变、其他非经典突变(包括E709X和L747X),至治疗失败时间(TTF)分别为12.6个月、11.5个月和10.7个月(图1),ORR分别为59%、64%和64%,对某些特定外显子20插入亚型(A763、M766、N771、V769)和奥希替尼耐药突变(G724S、L718Q、L718V、C797S)也有活性。
今年,一项来源于日本的II期科学研究显示,EGFR主要非经典突变对奥希替尼比较敏感。G719X(n=19)、L861Q(n=9)和S768I(n=8)突变患者的ORR各自为53%、78%和38%,PFS分别为8.2个月、15.2个月和12.3个月。
NEJ002研究的亚组分析显示,EGFR G719X、S768I、L861Q突变对吉非替尼不敏感,ORR仅为20%[12]。III期临床研究NEJ009证实[13],在EGFR突变阳性的晚期初治NSCLC患者中,吉非替尼联合含铂双药化疗方案对比单用TKI,ORR、PFS、OS明显延长,毒副作用加倍、但总体可耐受。由此可大胆推断,EGFR-TKI联合化疗,甚至联合贝伐单抗,在非经典突变中可能合理,但是仍需要进一步临床数据支持、验证。
一项韩国的多中心、前瞻性、单臂、开放标签II期研究KCSG-LU15-09证实,EGFR主要非经典突变患者对奥希替尼有效[14],19例患者携带G719X突变,ORR为53%,中位PFS为8.2个月;9例携带L861Q突变,ORR为78%,中位PFS为15.2个月;8例携带S861I突变,ORR为38%,中位PFS为12.3个月;4例患者携带了复合型突变(2例患者携带G719X + L861Q、2例患者携带S768I + G719X),4例患者中3例患者使用奥希替尼有效。
目前尚无前瞻性研究探索达克替尼和厄洛替尼在EGFR非突变患者中的疗效。
基于目前的研究结果,阿法替尼或者奥希替尼被推荐用于携带EGFR主要非经典突变的初治晚期NSCLC患者的一线治疗。尽管阿法替尼或者奥希替尼在EFGR非经典突变伴有脑转移的患者中均被证实有效,且均可降低脑转移风险,但研究数据十分有限,需要更多深入探索。
参考文献:
[1]. Chan, B.A. and B.G. Hughes, Targeted therapy for non-small cell lung cancer: current standards and the promise of the future. Transl Lung Cancer Res, 2015. 4(1): p. 36-54.
[2]. Costa, D.B., Kinase inhibitor-responsive genotypes in EGFR mutated lung adenocarcinomas: moving past common point mutations or indels into uncommon kinase domain duplications and rearrangements. Transl Lung Cancer Res, 2016. 5(3): p. 331-7.
[3]. Passaro, A., et al., Recent Advances on the Role of EGFR Tyrosine Kinase Inhibitors in the Management of NSCLC With Uncommon, Non Exon 20 Insertions, EGFR Mutations. Journal of Thoracic Oncology, 2021. 16(5): p. 764-773.
[4]. Russo, A., et al., Heterogeneous Responses to Epidermal Growth Factor Receptor (EGFR) Tyrosine Kinase Inhibitors (TKIs) in Patients with Uncommon EGFR Mutations: New Insights and Future Perspectives in this Complex Clinical Scenario. Int J Mol Sci, 2019. 20(6).
[5]. Gristina, V., et al., The significance of epidermal growth factor receptor uncommon mutations in non-small cell lung cancer: A systematic review and critical appraisal. Cancer Treat Rev, 2020. 85: p. 101994.
[6]. Zhang, T., et al., Treatment of uncommon EGFR mutations in non-small cell lung cancer: new evidence and treatment. Transl Lung Cancer Res, 2019. 8(3): p. 302-316.
[7]. Park, K., et al., Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomised controlled trial. Lancet Oncol, 2016. 17(5): p. 577-89.
[8]. Ramalingam, S.S., et al., Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC. N Engl J Med, 2020. 382(1): p. 41-50.
[9]. Yang, J.C., et al., Afatinib for the Treatment of NSCLC Harboring Uncommon EGFR Mutations: A Database of 693 Cases. J Thorac Oncol, 2020. 15(5): p. 803-815.
[10]. Kobayashi, Y. and T. Mitsudomi, Not all epidermal growth factor receptor mutations in lung cancer are created equal: Perspectives for individualized treatment strategy. Cancer Sci, 2016. 107(9): p. 1179-86.
[11]. Yang, J.C., et al., Clinical activity of afatinib in patients with advanced non-small-cell lung cancer harbouring uncommon EGFR mutations: a combined post-hoc analysis of LUX-Lung 2, LUX-Lung 3, and LUX-Lung 6. Lancet Oncol, 2015. 16(7): p. 830-8.
[12]. Watanabe, S., et al., Effectiveness of gefitinib against non-small-cell lung cancer with the uncommon EGFR mutations G719X and L861Q. J Thorac Oncol, 2014. 9(2): p. 189-94.
[13]. Hosomi, Y., et al., Gefitinib Alone Versus Gefitinib Plus Chemotherapy for Non-Small-Cell Lung Cancer With Mutated Epidermal Growth Factor Receptor: NEJ009 Study. J Clin Oncol, 2020. 38(2): p. 115-123.
[14]. Cho, J.H., et al., Osimertinib for Patients With Non-Small-Cell Lung Cancer Harboring Uncommon EGFR Mutations: A Multicenter, Open-Label, Phase II Trial (KCSG-LU15-09). J Clin Oncol, 2020. 38(5): p. 488-495.




















