sglt2抑制剂类降糖药物
药渡ZL荟【ZL分析】第五个专题,我们将关注热门靶点及其重点药物的ZL分析。
刚刚过去的11月14日,是国际糖尿病日,根据国际糖尿病联盟的统计,2015年全球约有4.15亿患者,到2040年这一数字将达到6.41亿人次。中国是成人糖尿病患者最高的国家,糖尿病患者高达1.1亿。
降糖药一直是药企们研发的重点,前两年的DPP4抑制剂火热渐渐退去,近期SGLT-2抑制剂走到台前,颇受关注。
SGLT2抑制剂持续升温
SGLT2,全称sodium-glucose co-transporter 2,钠-葡萄糖协同转运蛋白。SGLT2抑制剂使肾小管中的葡萄糖不能顺利重吸收进入血液而随尿液排出,从而降低血糖浓度。
优势:由于其不干扰胰岛素和胰高血糖素分泌调节通路,所以引起低血糖的可能性相对较小。众多研究显示,SGLT2抑制剂可有效降低糖化血红蛋白。对于经饮食和锻炼控制不佳的 2 型糖尿病,SGLT2抑制剂不仅可有效改善血糖,还可降低体重和改善血脂。
前景:据Evaluate Pharma预测,到2022年,SGLT2抑制剂类药物将凭借132.6亿美元的全球销售额,一举成为第三大糖尿病治疗药物。与此同时,有两只SGLT2抑制剂将跻身全球糖尿病治疗药物前5强,分别是2022年全球销售额为39亿美元的恩格列净和37.1亿美元的卡格列净(Invokana)。尤其是前者恩格列净,6月29日,FDA的顾问小组以12-11的投票赞成恩格列净能够降低心血管死亡的风险的说法。鉴于此,对于勃林格殷格翰与礼来而言,双方都将着手开展恩格列净心血管益处的营销策略。该项试验的结果无疑将很快出现在治疗指南中,这将提升该药的市场需求,甚至是整个SGLT2抑制剂类别(参考资料来自医药经济报)。
目前,已有六个SGLT2抑制剂类药物被批准上市,ZL作为利益之油,是销售额的重要保证。下面针对SGLT2抑制剂重点品种,详解ZL保护情况。
SGLT2抑制剂类重点上市药物ZL分析
1Empagliflozin 恩格列净
Jardiance® (恩格列净,Empagliflozin),最初由勃林格殷格翰研发,后期和礼来联合开发,于2014年5月22日首先获得欧洲药物管理局(EMA)批准上市,之后于2014年8月1日获得美国FDA的批准,又于2014年12月26日获日本药品与医疗器械管理局(PMDA)批准上市。
化合物ZL:
Jardiance®的化合物ZL于2005年以国际ZL申请方式,即PCT申请公布,(公开号WO2005092877A1)进入各个国家后,并陆续在美国、日本、欧洲以及中国等药品主流市场获得授权,并在美国获得235天的延长期(Patent term adjustment),ZL到期日为2025年11月5日,在日本获得5年的延长期(受益于新药ZL补偿制度),ZL到期日为2030年3月11日,见表1。

表1 Jardiance®化合物ZL在药品主流市场的保护情况
注:*表示ZL期延长
作为NCE获得批准,Jardiance®在美国获得了5年的市场独占期。随后恩格列净的复方制剂也相继获得批准,分别为与利格列汀(Linagliptin)联合用药的Glyxambi®和与二甲双胍联合用药的Synjardy®,其中二甲双胍为抗糖尿病的基础一线用药,利格列汀为Boehringer Ingelheim开发的DPP-4抑制剂,其单方制剂在2011年获得FDA批准。从表2中我们可以看出在2014年和2015年短短两年的时间,Boehringer Ingelheim的抗糖尿病产品线上市了四个品种,以此来一步步扩大市场占有率。

表2 恩格列净相关品种FDA获批情况
外围ZL保护:
继化合物ZL后,在研发过程中,原研公司陆续申请了与Jardiance®相关的外围ZL。Jardiance®以游离态的形式作为活性药物成分,因此,盐类ZL不是其ZL布局关注的重点,在申请化合物ZL后,除了一个晶型ZL(公开号WO2006117359A1),原研公司重点申请了适应症和联合用药ZL。适应症中除用于预防、延迟或治疗代谢障碍包括:Ⅰ型糖尿病、Ⅱ型糖尿病、高血糖症、肥胖症、代谢综合征等,还特别申请了因使用精神安定剂治疗而诱发的代谢障碍和肾损伤的糖尿病患者等多适应症ZL。因糖尿病治疗的最终解决方案往往是联合用药,且目前为止已开发出多种作用机制不同的降糖药物,协同加强效果,互补完善机制,因此和不同靶点药物的联合用药的ZL布局也成为抗糖尿病药物的一大特色。其中WO2008055940A2中保护了和二甲双胍、格列美脲、噻唑烷二酮、米格列酮的联合用药, WO2010092124A1保护了和利格列汀(Linagliptin)的联合用药。
在中国,原研公司通过PCT申请的ZL大部分进入中国(见表3),化合物ZL早在2006年就已进入中国,但直到2015年CN103450129B才获得授权,且授权版本中仅保护了Jardiance®的结构式和其对应异构体,查看相关的审查意见,得知原申请文件中权利要求1-13不具备创造性,不符合ZL法第22条第3款的规定,进而对权利要求作出了相应修改。原申请权利要求1请求保护若干个吡喃葡萄糖取代的苯基衍生物,根据说明书记载,其可作为SGLT2抑制剂,而对比文件1(CN1407990A,2003/4/2)公开了同样作为SGLT2抑制剂的化合物(该化合物为2014年BMS上市的达格列净),其区别技术特征仅为部分取代基不同,见图1,然而在对比文件1的基础上结合本领域的常规实验手段得到权利要求保护的技术方案是显而易见的,即权利要求1不具备突出的实质性特点和显著的进步。

图1
除化合物ZL获得授权外,晶型和制备方法的相关ZL也陆续获得授权,见表3。晶型ZLCN101155794B中保护了化合物的一种稳定晶型,满足对于药物活性物质的重要要求。制备方法中有3项获得授权,分别对恩格列净、中间体、晶型的制备方法进行了保护。

表3 Jardiance®在中国的ZL保护情况
2Tofogliflozin 托格列净
Deberza®/Apleway® (Tofogliflozin,托格列净)由Chugai研发(2002年被Roche收购),2012年Chugai,Kowa和Sanofi三方达成共识共同开发该产品,2014年3月24日获得PMDA批准上市,由Sanofi和Kowa分别以不同的商品名上市销售(以下统一用Deberza®)。2015年9月Chugai宣布将Deberza®在美国和欧洲的开发权将授予Kowa,并获得巨额的特权使用费。
化合物ZL:
Deberza®化合物ZL于2006年以国际ZL申请方式,即PCT申请公布(公开号WO2006080421A1),进入各个国家后,并陆续在美国、日本和中国获得授权,且在美国获得了369天的延长期,ZL到期日为2027年1月31日。而进入欧盟国家阶段的ZL申请仍处于实审状态,见表4。

表4 Deberza®化合物ZL在药品主流市场的保护情况
注:*表示ZL期延长
外围ZL保护:
除了上述的基础ZL之外,为了分析原研公司如何构筑ZL壁垒,利用ZL之盾捍卫自身的利益,笔者进一步调研了原研公司的全球布局情况。见表5.首先具有良好的理化学性质是成药的必要的特征,对此原研公司对其晶型进行了较为严密的布局,WO2009154276A1重点保护了一水合物晶型和两种共晶物,WO2012115249A1则保护了一种Ⅱ型结晶,期望通过此种手段为产品赢得更长的保护期。其次,多种作用机制不同的降糖药物形成联合用药,以产生更好的疗效,这是对药物进行深度开发的常用手段之一,对此,与其他抗糖尿病原研公司不约而同地,Sanofi对Tofogliflozin也进行了联合用药的ZL布局。近年来,G蛋白偶联受体119(GPR119)成为糖尿病药物研发的新靶点,Sanofi公司研发了一系列该类产品,包括吡咯烷酮衍生物,茚酮衍生物,稠杂环衍生物,异吲哚啉酮衍生物等,并申请了相关ZL,ZL中重点保护了和SGLT2靶点药物的联合用药。

表5 Deberza®国际ZL申请的技术统计(ZL族)
在中国,原研公司通过PCT申请的ZL中仅有3项进入中国,其他大部分PCTZL还没有进入国家阶段。进入中国的3项ZL包括了化合物核心ZL,晶型及制备方法ZL,化合物ZL和晶型ZL已经获得授权,制备方法ZL处于实审中,见表6。其中晶型ZL(授权公告号CN102046645B)重点保护了一水合物晶型(Deberza®的API形式),ZL保护期至2029年。

表6 Deberza®在中国的ZL保护情况
-
科技前沿
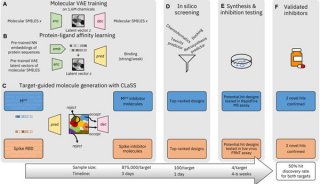
-
焦点事件

-
科技前沿
-
产品技术