DELFIA经典技术应用于单抗研发及细胞治疗(二)
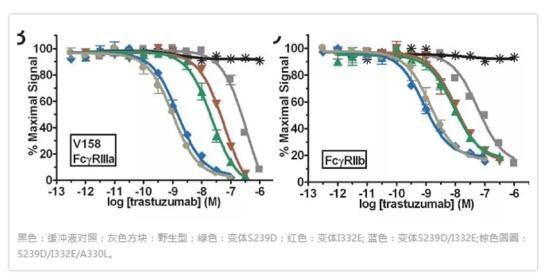
在亲和力筛选的基础上,研究利用DELFIA EuTDA-based cytotoxicity assay(货号AD0116)在细胞水水平探究变体对ADCC的提升。以不同FcγRIIIa基因型的PBMCs为效应细胞,Her2+ SkBr3为靶细胞,研究证明改造的变体能有效提升ADCC(2-3个数量级),与亲和力数据趋势一致(下图左)。进一步的研究证明变体能有效引发针对HER-2不同表达水平的细胞株的ADCC。针对几乎没有抗原表达的MCF7细胞系,变体依然具有客观的ADCC活力(下图右)。

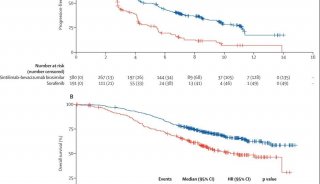
除了基因水平多态性外,Fc区域的糖基化也影响其和FcγR的亲和力。尤其是岩藻糖的缺失会提升IgG1和FcγRIIIa之间的亲和力。因此,除了突变外,改造Fc区域的糖基化修饰也是提升治疗性抗体ADCC活力的一个途径。以由罗氏研发的Lumretuzumab单抗(RG7116)为例[6]。RG7116一方面阻断HER3的激活并下调HER3的表达。进一步通过罗氏去岩藻糖修饰的GlycoMab技术改造,RG7116和FcγRIIIa之间的结合亲和力提高50倍。基于DELFIA技术的ADCC检测证明,糖基化改造显著提升RG7116的ADCC活力(下图左)。同时,对比不同HER3表达量的细胞系,研究清晰地表明HER3受体表达丰度和RG7116介导的ADCC活力之间的正相关联系(下图右)。在动物模型上,基于多种低免疫细胞浸润的小鼠皮下瘤模型,研究发现RG7116仅通过靶向HER3就能发挥抗癌作用。进一步利用高免疫细胞浸润的异种原位移植A549肺癌小鼠模型,研究证明糖基化改造有效提升小鼠的生存周期。临床一期试验进一步证明RG7116的临床疗效。一方面,RG7116有效抑制了肿瘤细胞膜HER3的表达。同时,相较于未糖基化改造的抗体,RG7116升高外周NK免疫细胞的活化程度[7]。

免疫治疗领域之首个PD-1抗体: Nivolumab
虽然同是单抗药物,PD-1抑制剂与常见的靶向药物作用机制不同。PD-1抗体主要用于阻断PD-1和其配体PD-L1的相互作用,而不是杀伤PD-1阳性细胞,也就是抗肿瘤效应细胞。在Nivolumab的体外表征分析研究中,DELFIA Cell Cytotoxicity Kit(货号AD0116)被用于确认Nivolumab是否会诱导ADCC产生。以活化的PBMCs为效应细胞,高表达PD-1的CD4阳性细胞为靶细胞,研究人员确认IgG4亚型的nivolumab不会诱发ADCC效应[8]。后续的实验进一步证明nivolumab不能介导CDC,因此nivolumab的引入不会清除PD-1阳性细胞群体。除了nivolumab外,其他的PD-1单抗,包括默沙东的Keytruda、百济神州的BGB-A317及恒瑞的SHR-1210,都为弱ADCC活性设计。然而,同样是免疫检查点抑制剂,CTLA-4单抗Ipilimumab则需要其ADCC活性来杀伤Treg细胞发挥作用,强调了不同作用机制对抗体ADCC活性的要求也有区别[9]。

ADCC活力的检测不仅能协助解析单抗药物的MOA,也推动对于NK细胞功能的研究及开辟新的抗肿瘤策略。作为成熟的细胞杀伤检测工具,DELFIA® EuTDA(货号AD0116)细胞毒法不仅可用于评估抗体的ADCC和CDC活力,还能用于检测ACT,CAR-T和CAR-NK等疗法中免疫细胞的杀伤能力。为了助力免疫治疗的开发,我们近期推出“珀金埃尔默生命科学试剂耗材平台”,加速您的研究和药物开发进程。