Alnylam制药公司Onpattro 获日本批准,治疗hATTR淀粉样变性
近日,Alnylam制药公司宣布,日本卫生劳动福利部(MHLW)已批准Onpattro(patisiran),用于成人患者治疗由遗传性转甲状腺素蛋白(hATTR)介导的淀粉样变性引起的多发神经病。Onpattro是日本批准的首个RNAi疗法,Alnylam公司已计划在日本立即推出该产品。在美国和欧盟,Onpattro分别于2018年8月10日和8月30日获批。
Onpattro的获批,基于III期临床研究APOLLO的数据。这是一项随机、双盲、安慰剂对照、全球性研究,在伴发多发性神经病的hATTR淀粉样变性患者中开展,旨在评估patisiran的有效性和安全性。研究共入组225例患者,涵盖39个基因型。研究中,患者以2:1比例随机分配至patisiran(0.3mg/kg,每3周静脉输注一次)和安慰剂治疗。主要终点是治疗第18个月改良神经病变损害评分(mNIS+7)相对基线的变化。mNIS+7是一种神经功能缺损的综合衡量工具,评估感觉运动能力、神经传导、反射和自主功能。次要终点包括Norfolk QOL-DN生活质量评分以及运动强度(NIS-W)、残疾(R-ODS)、步速(10米步行测试)、营养状况(mBMI)和自主神经症状(COMPASS-31)。探索性终点包括:存在基线心肌受累的患者中的心脏测量,以及皮肤活组织检查中皮肤淀粉样负担和神经纤维密度的测量。对于mNIS+7和Norfolk QOL-DN测量,较低分数意味着更好的临床结果。
研究结果显示,patisiran取得了极佳的治疗效果,达到了研究的主要终点和所有次要终点:与安慰剂相比,patisiran改善了多神经病、生活质量、日常生活活动能力、步行能力、营养状况、自主神经症状。此外,在心肌受累的患者(占研究患者总数的56%)中开展的一项心脏亚组分析结果显示,与安慰剂相比,patisiran在心脏结构和功能探索性终点方面也表现出显著改善。安全性方面,patisiran治疗组和安慰剂组不良事件发生率和严重程度均相似,patisiran治疗组周围水肿和输液相关反应发生率较高,但通常是轻至中度。
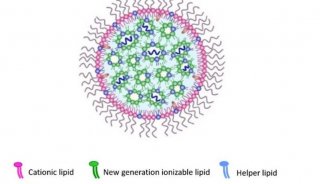
Onpattro是一种通过静脉注射的RNAi药物,靶向甲状腺素运载蛋白(TTR)。Onpattro旨在靶向并沉默特异的信使RNA(mRNA),阻断TTR蛋白的生成,这可能有助于减少沉积并促进TTR淀粉样蛋白在外周组织中的清除,并恢复这些组织的功能。
业界对Onpattro的商业前景也十分看好。医药市场调研机构EvaluatePharma预测,Onpattro在2024年的销售额将达到13.08亿美元。
-
科技前沿
-
焦点事件
-
项目成果

-
项目成果
-
产品技术
-
产品技术