单细胞和TCR测序揭示了调节性T细胞的表型图谱
前言
CD4+调节性T细胞(Treg)在保持体内免疫平衡中起关键作用,他们的表型异质性反映了环境多样性以及它们所调节的靶细胞的多样性。因此,本文以小鼠的淋巴组织和人血为材料,用单细胞转录组、激活检测和TCR分析来探究调节性T细胞和传统的CD4+FoxP3-T细胞(Tconv)的表达谱。
实验方法
1、实验材料:小鼠、人-血
2、single-cell RNA-seq方法:Indrop, CEL-seq, 10X Genomics
结果与分析
1.CD4+ Treg和Tconv scRNA-seq数据分析
为了发现细胞的小亚群和特异性基因,对Treg和Tconv做了Indrop单细胞转录组分析。用流式细胞仪从Foxp3gfp小鼠中分选出CD4+TCRβ+GFP+Treg和GFP-Tconv细胞用于单细胞转录组文库构建(Fig.1a)。为了降低不同实验批次的影响和评估实验结果的稳定,本文还用了10XGnomics和CEL-seq的方法进行单细胞转录组实验。

Fig. 1 | Tregand Tconv scRNA-seq datasets
每个单细胞中检测到了1751unique mRNA分子(代表787gene),共检测到16720genes(Fig.1b)。与预期一致,2个重要的Treg marker--Foxp3和Il2ra在不同的Treg细胞中表达,但在Tconv细胞中几乎未表达(Fig.1c)。
2、CD4+ Treg和Tconv细胞之间的转录关系
用tSNE分析Treg和Tconv细胞的转录情况,发现Treg主要分布在D区,Tconv主要分布在E区,但他们也有一些重叠,如在E区发现了一些Treg细胞(‘furtive’Tregs),反之亦然。大部分’furtive’Tregs可以检测到Foxp3表达,且和其他的Tregs表达水平相似(Fig.2c)。
在E区,Tregs的信号基因过表达,表达量远高于Tconv细胞;但在E区之外,Tregs的信号过表达转移到了Il2ra和Ikzf2等基因。

对分散区域(A-C区)的基因表达进行分析,在A区发现Tregs和Tconvs过表达基因与B细胞淋巴结相关(如Tfollicular helper (Tfh)和Tfrcells);在B区,Tregs和Tconvs的上调基因与TCR的早期响应有关(Nr4a1, Egr1, Egr2,Myc and Dusp2),表明在这两种细胞中TCR可能有相似的启动程序。
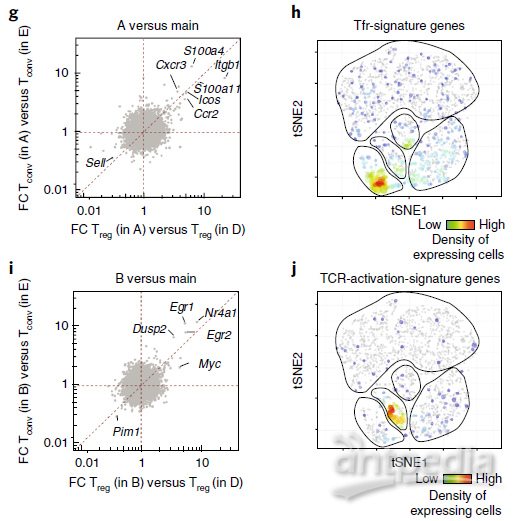
Fig.2 | Some Tregs and Tconvs show closely relatedtranomes.
d,e,f中的红色-上调,蓝色-下调
3、脾脏Treg 细胞的异质性围绕着几个不同的极点
如图a,b所示,将脾脏Treg细胞分为6个clusters。作者分析发现,cluster4-6中的Treg细胞可能处于休眠状态,而cluster1-3中的Treg细胞可能处于激活状态(通过一些与Treg细胞休眠相关基因的表达水平判断,Sell,Ccr7)。此外,cluster1-3可代表激活表型的2个极点,cluster3中细胞主要表达早期细胞激活的基因(Nr4a1, Egr1, Egr2,Dusp2),从而诱发了TCR-mediated激活。
根据a中定义的基因的表达推测每个单细胞可能的状态做CAP图(图c),大部分Treg细胞能清晰地投射到一个主簇中,尤其是处于激活状态的cluster1-3,而cluster4较分散。tSNE图发现休眠状态的cluster映射到核心Treg区域,而激活的cluster映射到与Tconvs重叠的边缘区域(A-C),表明Treg激活导致了与Tconvs的部分重叠。

scRNA-seq数据预测CXCR3主要由CD62Llo激活的T细胞显示,且CXCR3和NR4A1在很大程度上相互排斥。这些预测最终被证实,CXCR3在CD62lloTregs上表达,CXCR3在NR4A1-Tregs上表达最高。对Treg细胞效应分子表达频率和分布情况进行判定,发现效应分子的表达无相互排斥,且鉴定出一个共表达效应分子。Il2ra和Ctla4是最常见的抑制分子。相反,Lrrc32和Tgfb1存在相互偏好性表达。Il10和Areg在激活的簇中优先表达,但非常罕见,这与它们优先部署在组织Tregs或炎症部位相一致。因此,脾脏Treg细胞采用连续的状态,围绕一个休眠状态和2个激活状态,从而有独特的表型和效应功能。

Fig. 4| Resting andactivated Treg states identified by scRNA-seq
4、TCR 信号在影响Treg细胞状态中的作用
Nr4a1是一种转录因子,在T细胞激活时Nr4a1的表达以与TCR信号强度成正比的方式被快速诱导。因此作者利用Nr4a1gfp报告小鼠,并结合Treg单细胞数据将GFP的表达分为3个区,发现Nr4a1的出现频率和表达水平与Treg细胞的来源一致。不同Nr4a1表达水平的Treg细胞形成了一个从低到高表达的轨迹。

Fig. 5 | Tregstates associated with different TCR-signaling strength
激活的Treg分布随NR4A1-GFP强度的改变而显著变化,cluster3中的细胞比例随GFP增加,而cluster1和2中的细胞比例降低。
因此,在生理环境和没有炎症刺激的情况下,TCR信号水平不影响激活的Treg细胞的比例,但显著地扭曲了它们的表型选择。
5、人和鼠的Treg细胞有相似的异质性模式
最后,作者研究了小鼠脾脏Treg的结论是否也适用于人类细胞。用流式分选出人血液的Treg和Tconvs细胞,并进行scRNA-seq。Treg和Tconvs细胞之间的异质性和相互关系及其基因表达等方面,与小鼠的结果非常相似。
Treg和Tconvs细胞簇是分开的,但furtiveTregs 存在于Tconvs细胞的的主要区域(A区,高达55%,鼠的只有26%)。furtiveTregs 细胞也表达了FOXP3,尽管其表达水平低于其他的Tregs细胞。



Fig. 6 |Similitudes in human and mouse Treg heterogeneity
参考文献
AZemmour, D., Zilionis, R., Kiner, E., Klein, A. M., Mathis, D., & Benoist, C. (2018). Single-cell gene expression reveals a landscape of regulatory T cell phenotypes shaped by the TCR. Nature immunology, 19(3), 291-301.
- END -
本文系欧易生物原创
转载请注明本文转自欧易生物
-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章







