ADC 单抗药物的分子量、氨基酸序列、糖基化位点以...(二)
2.1.3 数据分析方法
采用 Protein Deconvolution 2.0 软件对原始质谱图进行去卷积处理,得到完整的蛋白质分子量信息。
2.2 氨基酸序列、糖基化位点和 ADC 药物结合位点测定
2.2.1 仪器和试剂
质谱仪器:Q-Exactive(赛默飞世尔科技,美国);
色谱仪器:Accela 液相色谱系统(赛默飞世尔科技,美国);
色谱柱:Thermo Scientific, C18, 100Å ,1.9 μm, 2.1×100 mm
试剂:二次去离子水,色谱级乙腈,色谱级甲酸。
2.2.2 仪器方法
色谱分析条件:具体见表 3;
表 3. 氨基酸序列测定的色谱分析条件
流动相 | A:0.1% 甲酸水溶液;B:0.1% 甲酸乙腈溶液 | |
流速 | 300 μL/min | |
柱温 | 35℃ | |
色谱梯度 | 时间/min | B相浓度/% |
0 | 5 | |
4 | 5 | |
45 | 35 | |
50 | 90 | |
52 | 90 | |
52.5 | 5 | |
60 | 5 |
质谱分析条件:具体见表 4;
表 4. 氨基酸序列测定的质谱分析条件
喷雾电压 | 3.5 kV |
毛细管加热温度 | 275℃ |
S-lens | 60 %; |
碰撞能量 | 27% 归一化能量 |
碎裂方式 | HCD |
质量扫描范围 | m/z 300–1800 |
分辨率 | 一级35,000(m/z 200), |
二级17,500(m/z 200) |
2.2.3 数据分析方法
采用 Proteome Discoverer 1.3 软件对原始谱图进行数据库搜索,具体搜库参数为:包含单抗氨基酸序列的数据库;半胱氨酸(C)烷基化(+57.021Da)设置为固定修饰;甲硫氨酸(M)氧化(+15.995Da)、天冬酰胺(N)和谷氨酰胺(Q)脱氨基化(+0.984Da)、赖氨酸(K)ADC结合(+956.3644Da)、天冬酰胺(N)G0F糖基化(+1444.5300Da)设置为可变修饰;trypsin 设置为酶;酶漏切位点为 2。
3. 结果与讨论
3.1 蛋白质分子量测定
基于高分辨质谱 Q-Exactive,为了保证采集谱图的质量和数量,我们设定 Orbitrap 检测器的采集分辨率为 17,500。经过 Q-Exactive 质谱采集的 ADC 单抗药物的原始色谱质谱总离子流图和原始质谱图如图 2 和 3 所示,我们可以观察到 ADC 抗体药物在整个质量范围内表现出均匀的电荷分布,不同电荷的质谱峰之间可以实现基线分离,从而可以判断质谱的灵敏度、分辨率和信噪比都很高。同时选取强度较高的几组质谱峰进行放大,放大之后的几组质谱峰显示相似的分布模式。
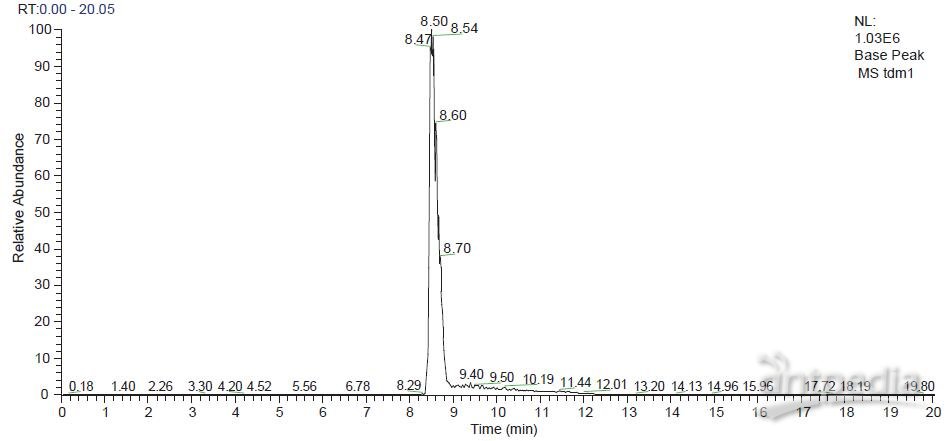
图 2. ADC 抗体药物色谱质谱流出图

图 3. ADC 抗体药物原始质谱图(红色虚线框内为中间几组峰的放大图)