颅内Castleman病病例分析
患者女,32岁。于2017年1月初无明显诱因出现头痛,为发作性胀痛不适,3~5min自行缓解,无头晕、呕吐、行走不稳、肢体无力、肢体麻木、口角抽搐、意识不清、听力下降、视物模糊。
MRI表现:T1WI呈等信号,T2WI呈中等偏高信号,DWI呈稍弥散受限,增强扫描呈明显强化,与脑组织以线样低信号影分界,与硬脑膜呈宽基底相连,其脑膜尾粗、长;右侧颞、顶叶大脑受压,皮质向内凹陷,右侧颞、枕、顶叶见大片状水肿带,右侧侧脑室后角受压,中线稍向左偏移。
CT表现:右侧颞顶部见一规则高密度影,与硬脑膜宽基底相连,边界清楚,平扫CT值约50HU,增强扫描明显强化,CT值约110HU,邻近颅骨骨质结构破坏吸收,周围见明显水肿带(图1~8)。
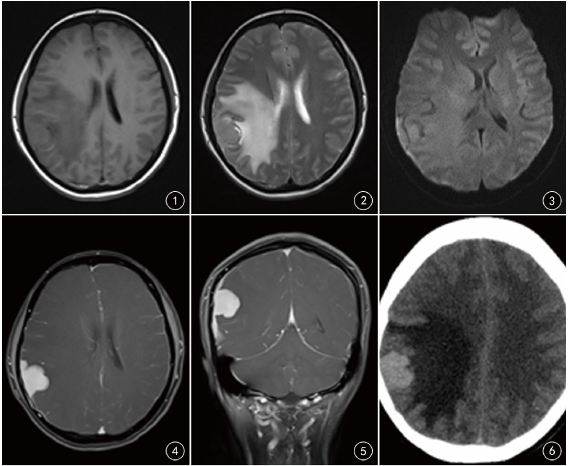
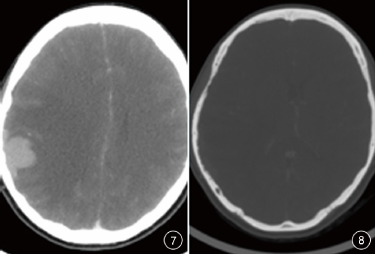
图1T1WI呈中等稍高信号;图2T2WI呈等信号;图3DWI表现为弥散稍受限;图4增强扫描轴位,强化明显;图5增强扫描冠状位,可见明显脑膜尾征;图6CT平扫表现为高密度影;图7CT增强扫描明显强化;图8CT骨窗可见骨质破坏吸收;
术中见脑内肿瘤突出脑组织表面,张力较高,与周围水肿带分界不清,肿瘤向前、向下沿硬脑膜弥漫生长。术后病理提示:右侧颞顶叶符合巨淋巴结增生(Castleman病),镜下见(右侧颞顶)淋巴组织增生,淋巴滤泡大小不等,滤泡中央可见硬化血管,滤泡周围可见呈同心圆排列的淋巴细胞,血管内皮增生,较多浆细胞和组织细胞浸润。免疫组织化学示:Vim(+),淋巴细胞Bcl-2(+),CD3(+),CD20(+),浆细胞CD38(+),CD138散在(+),组织细胞CD68(+),S-100(-),CD34(-),GFAP(-),EMA(-),PR(-),Ki-67约40%(+)(图9)。
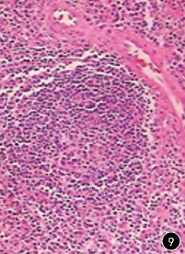
图9可见淋巴滤泡增生,滤泡中央可见硬化血管,滤泡周围可见呈同心圆排列的淋巴细胞,血管内皮增生(HE×200)
讨论
巨淋巴结增生症是一种少见良性增生性疾病,病因不明,据文献报道可能与血管内皮因子、EB病毒感染、HHV-8感染及细胞因子调节异常有关,现更多学者认为其发生与HHV-8感染及白细胞介素-6增多有关,1956年由Castleman等首先报道此病。巨淋巴结增生症根据病理学特点将其分为三型:透明血管型(主要由增生的淋巴结及丰富的血管构成)、浆细胞型(主要由滤泡及滤泡间片状成熟的浆细胞构成)和中间型(为兼有两种类型的混合体)。
临床及影像上分为:局限型与弥漫型两种类型,其中透明血管型约占本病的80%~90%,浆细胞型约占本病的3%~10%。本病可发生于任何年龄、任何存在淋巴组织的部位,其中纵隔及肺门占60%~70%,颈部占10%~14%,腹部占5%~10%,腋窝占2%~4%。由于发生于颅脑罕见,国内尚鲜有文献报道,对其影像认识不足,本病术前与脑膜瘤鉴别困难。脑膜瘤其信号及密度可不均匀,增强扫描多见较明显强化,其脑膜尾多呈细线样改变,邻近骨质以增生改变多见,对颅骨呈骨质破坏者少见,脑膜瘤MRS可出现特征性Ala峰。
颅内Castleman病非常罕见,本例与另一文献报道均出现粗、长脑膜尾征,提示当诊断为脑外肿瘤及出现明显粗、长脑膜尾征时,不能除外该病可能,加做MRS可能有助于鉴别诊断。目前颅内Castleman尚未有报道行MRS扫描,其意义有待于进一步探索。







