氯化氢测定方法介绍--硝酸银容量法
一、原理
氯化氢被氢氧化钠溶液吸收后,在中性条件下,以铬酸钾为指示剂,用硝酸银标准溶液滴定氯离子,生成氯化银沉淀,微过量的银离子与铬酸钾指示剂反应生成浅砖红色铬酸银沉淀,指示滴定终点,反应式如下:
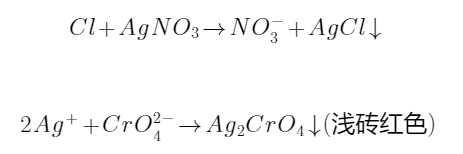
硫化物、氰化物、氯气及其它卤化物干扰测定,使结果偏高。
测定范围:40mg/m3以上。
二、仪器
①多孔玻板吸收瓶:75ml。
②棕色酸式滴定管:10或25ml。
③白瓷皿:75ml。
④烟气采样器。
三、试剂
①吸收液:氧氧化钠溶液C(NaOH)=0.10mol/L。
②络酸钾指示剂:称取5.0g铬酸钾,溶解于少量水,逐滴加入硝酸银溶液至产生少量淡砖红色沉淀为止。放置过夜,过滤,弃去沉淀,滤液用水稀释至100ml,贮存于棕色试剂瓶中。
③酚酞指示剂:称取0.50g酚酞,溶解于(1+1)乙醇100ml。
④硝酸溶液C(HNO3)=0.10mol/L。
⑤氯化钠标准溶液:用减量法称取0.55~0.60g氯化钠(优级纯,先在瓷坩锅中,于400~500℃灼烧至不再发出爆裂声,稍冷,移入称量瓶,称准至0.1mg),溶解于水,移入100ml容量瓶中,用水稀释至标线,摇匀。按下式计算其浓度:
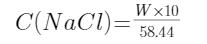
式中:C(NaCl)——氯化钠标准溶液的浓度,mol/L;
W——氯化钠的量,g;
58.44——1mol氯化钠的质量,g。
⑥硝酸银贮备溶液C(AgNO3)=0.10mol/L;称取17.0g硝酸銀,溶解于水,稀释至1000ml,贮于棕色细口瓶中。
标定:吸取氯化钠标准溶液10.00ml,置于白瓷皿中,加25ml水。加铬酸钾指示剂1.0ml,在玻棒不断搅拌下,用硝酸银贮备溶液滴定,至产生不消失的淡砖红色为止。记录硝酸银溶液体积(V)。
另取35ml水,同法进行空白滴定,记录体积(V0)。按下式计算浓度:
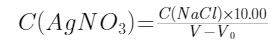
式中:C(AgNO3)——硝酸银贮备溶液浓度,mol/L;
C(NaCI)——氯化钠标准溶液浓度,mol/L;
V、V0——分别为滴定氯化钠溶液、空白溶液所消耗硝酸银贮备溶液的体积,ml。
⑦硝酸银标准溶液C(AgNO3)=0.01mol/L;吸取标定后的硝酸银贮备溶液10.00ml,置于100ml容量瓶中,用水稀释至标线,混匀,贮于棕色细口瓶中。
四、采样
按烟气采样方法的采样系统与装置,连接一支内装30~50ml吸收液的多孔玻板吸收瓶,以0.5L/min流量,采样5~30min。
五、步骤
①采样后,将样品溶液转入白瓷皿中,加酚酞指示剂1滴,滴加0.10moL/L硝酸溶液至红色刚刚消失。加铬酸钾指示剂1.0ml,在不断搅拌下,用0.01mol/L硝酸银标准溶液滴定,至产生不消失的浅砖红色为止。
②另取同体积吸收液,同法进行空白滴定。
六、计算
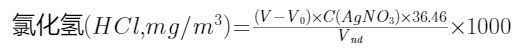
式中:V、V0——分别为滴定样品溶液、空白溶液消耗的硝酸银标准溶液体积,ml;
C(AgNO3)——硝酸银标准溶液的浓度,mol/L;
36.46——相当于1L 1mol/L硝酸银标准溶液(AgNO3)的氯化氢(HCl)的质量,g;
V——标准状态下干气的采样体积,L。
七、说明
①废气中含有氯化氢气体、盐酸雾及含氯化物的颗粒物时,木方法测定的是总氯离子含量,不能分别测定三者的浓度。
②氯化氢浓度高时,可串联两支吸收瓶采样,将样品溶液合并,定容后吸取适量溶液滴定。
③滴定时溶液应为中性或微碱性(pH6.5~10.5)。在酸性溶液中,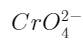 离子按下式反应而使浓度大大降低,影响终点时Ag2CrO4沉淀的生成。
离子按下式反应而使浓度大大降低,影响终点时Ag2CrO4沉淀的生成。
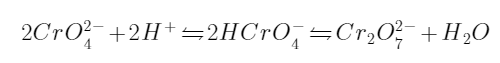
在碱性溶液中Ag+将形成Ag2O沉淀。
④废气中有氯气(Cl2)共存时,它与氢氧化钠反应生成等量的氯离子和次氯酸根离子,用碘量法测定次氯酸根,从总氯化物中减去其量,即得氯化氢含量。




















