颅内血管周细胞瘤的影像学特点及显微外科手术治疗
血管周细胞瘤(hemangiopericytoma,HPC),又称血管外皮细胞瘤,起源于叶间毛细血管Zimmerman细胞,是被WHO定义为Ⅱ-级的恶性肿瘤,颅内发生率不足中枢神经系统肿瘤的1%。以往对HPC的影像学特点认识不足,术前常被误诊为脑膜瘤,影响术前制定手术方案及手术疗效。
暨南大学医学院附属脑科医院神经外七科2012年1月—2018年1月采用手术治疗,并经病理证实、资料比较完整的颅内血管周细胞瘤患者26例。本研究对这26例HPC患者的临床资料进行总结分析,探讨其影像学特点和显微外科手术方法,以提高颅内HPC术前诊断水平和显微外科手术的疗效。
1.资料与方法
1.1一般资料
本组患者中,男15例,女11例;年龄23~60岁,平均年龄39岁;病史28d~13个月,平均6个月。临床表现为头昏、头痛者13例、头痛呕吐4例、癫痫3例、走路不稳4例、单侧上下肢无力2例。肿瘤位于大脑突面6例,大脑镰旁2例,镰窦旁3例,鞍区3例,前颅窝及中颅窝各2例,颅后窝4例,侧脑室、松果体区及小脑幕各1例,多发1例。
1.2影像学检查
本组患者术前均行颅脑MRI平扫+增强扫描,其中24例患者另行CT平扫和CTA检查,11例患者行DSA检查。MRI平扫显示,肿瘤边界清楚、形状不规则、呈分叶状;其中23例患者肿瘤内T1WI、T2WI信号不均匀,提示肿瘤内有过出血坏死;3例患者肿瘤内均匀信号;21例患者肿瘤内或肿瘤表面有迂曲血管流空影,以T2WI显示更清楚;21例患者瘤周有不同程度水肿,占位效应明显。MRI增强扫描显示,23例患者的肿瘤显著不均匀强化,3例患者均匀强化,2例患者有不典型脑膜尾征,3例患者的肿瘤不同程度累及上矢状窦。
24例患者CT检查显示,颅骨无变化者15例,肿瘤邻近颅骨溶骨性破坏者11例,全部患者均无肿瘤钙化。24例患者CTA检查显示,肿瘤为颈内外动脉双重供血,清楚显示肿瘤内及肿瘤外壁的供血动脉,其中17例患者肿瘤内有多发异常血管,提示肿瘤血运极为丰富。11例患者行DSA检查,肿瘤血运及供血动脉的显影比CTA更加清晰逼真,特别是进入肿瘤内的供血动脉显影更加清楚,对非常细小的肿瘤供血动脉也能显示。其中5例患者在DSA检查的同时行肿瘤供血动脉部分栓塞。
本组患者中,16例患者术前影像学诊断为HPC,与术后病理诊断一致;6例幕上HPC患者术前影像学诊断为脑膜瘤,4例颅后窝HPC患者术前影像学诊断为血管母细胞瘤。
1.3手术方法
根据影像学提供的信息设计手术入路和手术方法。本组患者中,单侧开颅者25例,双侧开颅者1例,均为骨瓣开颅。骨窗至少要大于肿瘤2cm,有利于充分暴露肿瘤和肿瘤供血动脉。26例患者术中均可看到肿瘤表面供血动脉,有的还能看到肿瘤的引流静脉;肿瘤呈灰红或暗红色,形态不规则,边缘不光滑,血运极为丰富,部分患者可看到肿瘤供血动脉搏动。
本组患者的颅内HPC基本都是以窄基底附着于硬脑膜,这一特点为较小肿瘤的切除提供了方便。术中可先用双极电凝阻断来自肿瘤基底部的供血动脉,然后离断肿瘤基底部,完整切除肿瘤。对于大型肿瘤直接暴露肿瘤基底部非常困难,可先细心分离肿瘤与周围组织的粘连,暴露出肿瘤的外壁,电凝肿瘤外壁的供血动脉,肿瘤引流静脉暂不阻断,留最后与肿瘤一并切除。肿瘤的大部分供血动脉被阻断后,用超声吸引囊内快速吸除肿瘤,剰余肿瘤囊壁分块切除,有效缩短肿瘤切除时间,减少出血。
本组患者中,有21例患者手术证实肿瘤内有坏死或囊变,与术前MRI检查结果一致;3例患者肿瘤累及上矢状窦侧壁,其中2例患者肿瘤侵蚀窦壁范围小,将受侵矢状窦壁连同肿瘤切除,用硬脑膜修补矢状窦,另1例患者因矢状窦受侵范围广未能全切除肿瘤。7例患者肿瘤侵蚀颅盖骨,很容易切除受侵颅骨及受侵硬脑膜,并切除正常颅骨及硬脑膜0.5~1cm。4例患者的肿瘤侵袭颅底,并累及颅底骨孔及经骨孔内的神经血管,无法完全切除肿瘤,电凝烧灼残留肿瘤组织。
颅底硬脑膜紧密贴符于颅底,无法将被肿瘤侵蝕的硬脑膜从颅底分离切除,用电凝反复烧灼以灭活肿瘤组织,被肿瘤侵袭的颅底骨也未能处理。术中所见HPC的血运极为丰富,貌似实体型血管母细胞瘤;因HPC为颈内外动脉双重供血,供血动脉数量常比血管母细胞瘤多,出血汹涌,均及时给予患者输血,补充血容量。本组患者术前均用神经导航对肿瘤进行精准定位,术中用神经导航引导;手术均在显微镜下进行。
2.结果
2.1术前影像学与术后病理诊断
本组患者中,术前影像学诊断为HPC,与术后病理诊断一致的患者16例(61.5%);6例幕上HPC患者术前影像学误诊为脑膜瘤,4例颅后窝HPC患者术前误诊为血管母细胞瘤,术后病理诊断均为HPC。
2.2手术效果及预后
本组患者中,肿瘤全切除者17例,次全切除者5例,部分切除者4例,无死亡患者。全部患者术后均行局部放射治疗。术后对患者随访6~42个月,平均28个月;一侧下肢无力4例,一侧上肢无力1例,走路不稳、共济运动失调3例。2年后1例患者肿瘤复发,3年后2例患者肿瘤复发。手术前后影像学对比,见图1-3。
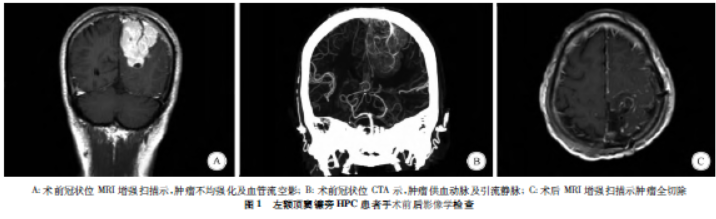

3.讨论
3.1颅内HPC的影像学特点
颅内HPC术前的影像学诊断很关键,对制定手术方案、提高手术疗效有重要价值。过去对颅内HPC的影像学表现认识不足,术前误诊率非常高。本组26例颅内HPC患者中,6例幕上HPC患者术前影像学检查误诊为脑膜瘤,4例颅后窝HPC患者均误诊为血管母细胞瘤;但误诊率明显低于有关文献报道。
颅内HPC术前误诊,对术前制定手术方案及治疗效果的评估都造成很大影响。近年来有学者,对颅内HPC的影像学特点进行了深入研究,使颅内HPC的术前诊断水平有显著提高。
本研究结合有关文献,对26例颅内HPC患者的术前影像学表现进行了回顾性分析。结果发现颅内HPC有以下的影像学特点:(1)MRI平扫显示肿瘤内常有出血,坏死及血管流空影;增强扫描肿瘤呈显著不均匀强化,以窄基底附着于硬脑膜,罕有脑膜尾征。(2)肿瘤边界清楚,形态不规则,呈分叶状。(3)CT检查显示肿瘤邻近颅骨常有溶骨性破坏,无颅骨增生,肿瘤无钙化。(4)血管造影显示肿瘤表面有迂曲粗大的供血动脉,部分患者出现肿瘤引流静脉;肿瘤内常见多发异常血管。
因颅内HPC的血运极为丰富,故影像学表现与同样血运丰富的脑膜瘤及实体型血管母细胞瘤有某些相似之处,常被误诊为脑膜瘤或血管母细胞瘤。本组26例HPC患者中,6例患者被误为脑膜瘤,4例患者被误诊为血管母细胞瘤就是例证。
3.2鉴别诊断
术前要仔细研读影像学检查资料,进行鉴别诊断。(1)HPC与脑膜瘤的鉴别:MRI平扫HPC有血管流空影,形态不规则,呈分叶状,增强扫描显著不均匀强化,肿瘤以窄基底附着于硬脑膜,罕有脑膜尾征,邻近颅骨常有溶骨性破坏,肿瘤无钙化。而脑膜瘤无血管流空信号,肿瘤边缘光滑无分叶,增强扫描呈均匀强化,肿瘤以宽基底附着于硬脑膜,多有脑膜尾征,无溶骨性破坏,肿瘤可有钙化。(2)HPC与血管母细胞瘤的鉴别:HPC常有颅骨溶骨性破坏,而血管母细胞瘤无颅骨破坏;脑血管造影显示HPC为颈内颈外动脉双重供血,而血管母细胞瘤只接受颈内动脉分支供血。
3.3手术方法及要点
颅内HPC的治疗方法首选手术切除;理想的治疗方案是手术全切除肿瘤+术后局部放射治疗。颅内HPC多位于大脑突面、大脑镰、静脉窦旁和颅底。术前要认真研究分析影像学资料,肿瘤相邻颅骨有否溶骨性破坏及程度,肿瘤有否累及头皮。详细了解肿瘤血运及肿瘤供血动脉的来源,以及这些供血动脉在肿瘤的位置;肿瘤与周围结构的关系等。
特别是肿瘤与大血管及重要功能区的关系。根据影像学检查提供的信息设计手术入路和肿瘤切除方法。术前用神经导航对肿瘤进行精确定位,术中用神经导航引导,可减少周围组织损伤,降低手术并发症,提高颅内HPC的手术治疗效果。总结本组26例颅内HPC患者的手术方法和效果,并结合有关文献分析,以下几点对降低手术风险、提高手术疗效、减少肿瘤复发至关重要。
3.3.1控制手术出血
手术骨窗要够大,因HPC是富血管性肿瘤,按通常大小骨窗不能满足手术需要。骨窗至少要大于肿瘤2cm,不仅有利于暴露肿瘤,更有利于控制手术出血。颅内HPC为颈内颈外动脉双重供血,供血动脉多而粗大,血运极为丰富,与颅内同样血运丰富的脑膜瘤比较,要比其血运丰富得多;手术风险也明显大于脑膜瘤。本研究的体会是颅内HPC不仅影像学表现貌似实体型血管母细胞瘤,术中所见也与实体型血管母细胞瘤很相似。肿瘤切除过程出血汹涌,术中要控制好出血,必要时及时输血补充血容量是手术成功的关键。
开颅时头皮、颅骨及硬脑膜动脉出血汹涌,要快速翻开皮瓣和骨瓣,也可同时将皮瓣与骨瓣一起翻开。迅速电凝出血的硬脑膜动脉,骨蜡涂抹骨缘止血;若骨缘出血汹涌骨蜡涂抹不上,可用电刀烧灼骨缘后涂抹骨蜡,止血效果良好。对于大型颅内HPC,直接暴露肿瘤基底部阻断肿瘤供血动脉非常困难,可先游离肿瘤与周围组织的粘连,暴露出部分肿瘤的外壁,电凝阻断走行于肿瘤外壁的供血动脉后,用超声吸引囊内快速吸除肿瘤,剩余肿瘤囊壁分块切除;可有效缩短手术时间,减少出血,降低手术风险。
3.3.2受累静脉窦的处理
矢状窦前1/3受累,不管矢状窦是否通畅,可将肿瘤与受累矢状窦一并切除;中后1/3矢状窦受肿瘤侵袭,若窦腔仍通畅,要尽可能切除受侵袭的矢状窦壁,并行修补;争取获得既完全切除肿瘤又保持矢状窦通畅的理想结果;且不可贸然切除矢状窦招致严重后果。若矢状窦完全闭塞可将肿瘤与受累矢状窦一并切除,这与矢状窦旁脑膜瘤切除原则相近,但又不完全相同。HPC是恶性肿瘤,在保证患者安全,不引发严重并发症的情况下,应尽量切除受累矢状窦壁,以减少肿瘤复发;需要时可用硬脑膜或脑膜修补材料修补矢状窦。
3.3.3受累颅骨及硬脑膜的处理
如前所述,HPC是恶性肿瘤,受肿瘤累及的组织要尽可能切除。受肿瘤累及的脑突面硬脑膜、大脑镰及颅盖骨与重要结构及功能区多无直接关连,基本都可以完全切除;必要时还可用人工修补材料替代。而肿瘤侵袭颅底,不仅侵袭颅底硬脑膜、颅骨及颅底骨孔,还侵袭及包裹穿行于骨孔内的神经和血管,根本无法完全切除肿瘤,受累颅底骨也难以切除;这时可电凝烧灼被肿瘤侵袭的颅底骨和颅底硬脑膜,尽可能灭活肿瘤组织,减少肿瘤复发。本组26例患者中,有11例患者术前行DSA检查,仅5例患者术前行肿瘤供血动脉部分栓塞。因病例少,故对肿瘤供血动脉栓塞患者术中的出血情况未作详细对比分析。
3.4术后放射治疗
颅内HPC是WHOⅡ-Ⅲ级的恶性肿瘤,手术治疗是首选方案。但由于肿瘤常累及颅底骨孔及骨孔内穿行的神经血管、静脉窦或功能区等重要结构,肿瘤很难以完全切除;即使肿瘤被完全切除,肿瘤仍有可能复发或转移,这是恶性HPC的性质所决定的。对颅内HPC术后应常规行局部放疗,以降低肿瘤复发率。本组26例患者术后均行局部放射治疗,术后随访3年多时间仅发现3例患者肿瘤复发,复发率明显低于文献报道的术后未进行常规放疗的HPC患者。




















