应用Orbitrap Fusion对TMT标记样本进行MS2定量方法...(一)
应用Orbitrap Fusion对TMT标记样本进行MS2定量方法以及SPS MS3定量方法的比较
1. 前言
目前,蛋白质组学研究已经由传统的大规模鉴定逐步转向了靶向蛋白质组学,研究内容已经由蛋白质鉴定扩展到了蛋白质相对和绝对定量,蛋白质相对定量方法中应用最普遍的为标记定量,包括:ICAT,DIART,ICPL,TMT,iTRAQ 等等,其中又以TMT 以及iTRAQ 的应用最为广泛。
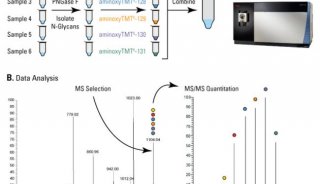
传统的TMT 以及iTRAQ 标记实验均使用MS2 碎片报告离子来进行定量,但是Steven P Gygi 等人发现该方法由于母离子筛选过程易受到基质干扰,因而定量结果与真实值相比偏低,而使用MS3 碎片报告离子来进行定量,则可以很好的解决这一问题,该方法的基本原理为:母离子碎裂产生的MS2 子离子用于定性,同时挑选碎片离子中强度最高的一个或者多个碎片离子,使用HCD 进行进一步的碎裂,产生的报告离子用于定量,虽然质谱在选择母离子时易受到基质的干扰,但是选择出来的母离子中绝大部分为目标母离子,因而MS2 子离子中强度较高的碎片离子绝大部分来自于目标母离子,挑选这些子离子的报告离子去做定量,定量结果会显著优于传统的应用MS2 碎片报告离子的定量方法。
本文主要介绍了赛默飞世尔新一代三合一高分辨质谱仪Orbitrap Fusion 应用SPS MS3 定量方法以及MS2 定量方法对TMT 标记样本进行定性与定量的实验,并对两种方法得到的结果进行了比较。结果显示:MS2 定量方法比SPS MS3定量方法可以鉴定并定量到更多的蛋白质,而SPS MS3 定量方法与MS2 定量方法相比可以鉴定并定量到更多低丰度的蛋白质,同时其定量结果也更加可靠。

2. 实验部分
2.1 样品信息
小鼠DC 细胞系,分别进行两种不同的处理,连同对照组,抽提蛋白质,酶解,分别使用TMT 标记为127,130,131,其中对照组标记为127,标记完成后,三种标记的样本混匀,使用pH10,RP 梯度进行分级,共得16 个馏分。
2.2 实验流程
样本使用A 液(0.1% FA,H2O)复溶,均上样4.5ul,60 min 色谱梯度分离,使用Orbitrap Fusion 对样本进行定性以及定量分析,质谱方法分别使用传统的MS2 定量方法以及SPSMS3 定量方法。
2.3 仪器条件
2.3.1 高效液相色谱条件
高效液相色谱仪:Thermo Scientific Easy-nLC 1000
色谱柱:Easy-spray column(C18 ,3 μm, 100Å ,75 μm×15 cm);
上样量:均4.5 μL
流动相:A: 0.1% Formic acid in water; B: 0.1% Formic acid in Acetonitrile
色谱梯度:
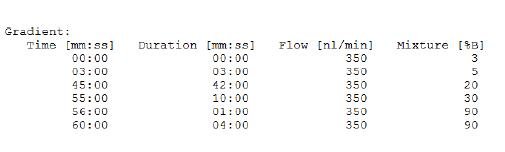
2.3.2 质谱条件
2.3.2.1 MS2 定量方法
质谱仪: Orbitrap Fusion
喷雾电压:2.1 kV
毛细管温度:275℃
S-lens:60%
碰撞能量:40% HCD
分辨率设置:一级120000@m/z 200,二级15000@m/z 200
母离子扫描范围:m/z 350-1800;子离子扫描范围:start
from m/z 100
Isolation Mode:Quadrupole
Data Dependent Mode:Top Speed
Cycle Time:3s
Exclusion Time:70s
2.3.2.2 SPS MS3 定量方法
质谱仪: Orbitrap Fusion
喷雾电压:2.1 kV
毛细管温度:275℃
S-lens:60%
Data Dependent Mode:Top Speed
Cycle Time:3s
Exclusion Time:70s
MS1: Orbitrap
分辨率:120000@m/z 200
扫描范围:m/z 400-1800
MS2: Ion Trap
Isolation Mode: Quadrupole
Activation Type: CID
Collision Energy:30%
MS3: Orbitrap
Precursor Exclusion:low:30,high:5
Number of Notches:10
Isolation Mode:Ion Trap
Activation Type:HCD
Collision Energy:65%
分辨率:30000@m/z 200
扫描范围:m/z 100-400