一例上腹部饱胀不适病例分析
患者女性,44岁,因反复上腹部饱胀不适两个月余入院。患者两个月前无明显诱因出现上腹部饱胀不适,反复发作,疼痛无节律,无恶心呕吐,无畏寒发热,无黑便。查体:肝、脾肋下未及,肝、脾区无压痛,脾未过中线。
入院血常规:白细胞7.1×109/L,红细胞5.14×1012/L,血红蛋白154g/L,血小板213×109/L。CT检查:脾脏形状与大小正常,脾脏内可见一大小约3.4 cm×4.4 cm低密度灶,平扫CT值约为33HU,动脉期病灶CT值约为170HU,静脉期约为160HU(图1~3)。

图1CT平扫横断位可见脾脏实质内低密度结节影(白箭),边界稍欠清晰;图2CT增强动脉期横断位可见病灶明显强化,边界清晰;图3CT增强门脉期横断位可见病灶密度接近周围脾脏实质;
拟诊:脾脏血管瘤可能。患者在本院于全身麻醉下行脾脏切除术。手术后病理大体:脾脏一个,大小约为10 cm×7 cm×3 cm,切面脾脏实质内见一暗红肿块,大小3.5 cm×2.5 cm×3.5 cm,质中,境界不清,见大小不一囊腔,直径0.2~0.8 cm,距脾脏包膜1 cm。
镜下观察:肿块有大量扩张呈血窦的囊腔,内衬扁平上皮,瘤细胞呈梭形,弥漫成片,与正常结构分界不清(图4)。免疫组织化学结果:肿瘤细胞Ⅷ因子++、CD68++、CD31++、CD34++、CD4+、Lyso++、Ki675%+(图5)。综合该患者临床特征、影像学特征及病理改变,最终诊断为脾脏窦岸细胞血管瘤(littoral cell angioma,LCA)。
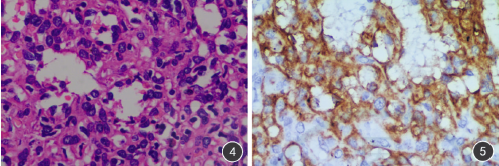
图4病理组织学观察可见大小不等、互相吻合的血管腔构成,内衬扁平上皮(HE×400);图5免疫组织化学观察可见窦腔壁内皮细胞CD31呈阳性(EnVision法×400)
讨论
脾脏LCA是一种罕见的、脾脏特有的血管源性肿瘤,来源于脾脏红髓内的窦岸细胞,由Falk于1991年首次提出。它具有同时表达内皮细胞与组织细胞相关抗原的特性,病因不明,可能是由于各种刺激因子如慢性感染或肿瘤所致。
组织学上,LCA组织由大小不等、相互吻合的窦样腔隙构成,腔壁上伴有突向腔内的乳头状突起或呈囊状扩张,腔隙壁及乳头状增生突起的表面均衬以单层立方或低柱状内皮样细胞。免疫检查显示LCA呈双重分化,即内皮细胞(CD31)及组织细胞(CD68)标志物均呈阳性,因此,免疫组织化学检查是确诊LCA的重要手段。
LCA可以发生于任何年龄,多见于30~50岁,无明显性别差异。有学者报道,LCA常伴有脾大、脾功能亢进等临床症状,还可出现发热、寒战、无力、疲劳、疼痛等症状,一部分患者为偶然发现或体检发现,并不伴有特殊临床症状。病变大部分为多发结节,少数为单发结节。
本例为44岁女性患者,因上腹部饱胀不适就诊,为单发结节。LCA是一种良性肿瘤,但也有其恶性生物学行为的报道,称作脾脏窦岸细胞血管肉瘤。有文献报道,30%的LCA病例合并身体其他部位的恶性肿瘤,如结直肠癌、肾癌、肺癌、胰腺癌等,合并淋巴瘤也比较常见。约17%的LCA病例合并自身免疫性疾病,如强直性脊柱炎、系统性红斑狼疮、银屑病、甲状腺机能减退、再生障碍性贫血等。因此,对LCA患者要进行详细的全身检查及密切的长期随访,及早发现伴随病变。
影像学上,LCA常见脾脏肿大,病变表现为脾脏实质内孤立或多发结节,直径1~6 cm,少数可弥漫累及全脾。与周围脾实质相比,CT平扫LCA一般表现为稍低密度,密度均匀或不均匀,未见钙化及包膜,有时表现为等密度,与正常脾实质不易区分。CT增强扫描LCA,表现为类似于脾脏血管瘤及脾脏错构瘤的渐进性增强方式,增强早期病灶显示为不均匀增强但较脾实质密度低的病灶。这种表现与LCA由不规则血管腔吻合构成有关。病灶边界一般较清晰,但也有边界不清或结节相互融合。
有研究表明,观察瘤灶数目最佳时期是增强扫描的门静脉期,延迟期病灶多表现为均匀等密度,与脾实质密度接近。本例病灶平扫表现为低密度,增强后显示病灶逐渐增强,动脉期明显强化,门脉期病灶与脾实质密度接近。笔者认为,CT检查诊断脾脏LCA,表现为脾脏单发或多发的大小不等的结节和肿块,增强后明显强化,且有延迟强化的特点,最后确诊需病理证实。




















