一例血管性水肿表现为系统性红斑狼疮病例分析
患者,女,32岁。因手背、嘴唇、右眼眶周肿胀入院。既往病史:原发性甲状腺功能减退症,持续6个月。用药左旋甲状腺素75 µg/d。否认在面部和手肿胀前接触过药物、食物、昆虫毒液和物理因素。既往无类似疾病,无血管性水肿家族史。既往病史不明显。
一般体格检查发现,患者个子高,瘦,无热。手背包括手指红肿,无压痛和硬结。与单侧眶周膨胀和红斑相关(图1),临时诊断为血管神经性水肿伴潜在的变态反应性疾病。临床检查未发现足或骶水肿、淋巴结肿大或肝脾肿大。体检无血管炎。实验室检查显示双血球减少,血红蛋白11.4 g/dL(正常范围10.7–14.9),白血细胞计数2.88*103/µL(正常范围3.30x103–9.66x103),绝对淋巴细胞计数0.9*103/µL(正常范围1.04*103–2.86*103/µL),血小板计数46*103/µL(正常范围150*103–450*103/µL)。红细胞沉降速率(ESR)30 mm/h(正常范围0–20 mm/h)。C1酯酶抑制剂(C1–INH)水平降低,180 mg/L(正常范围210–390 mg/L)。骨髓检查和血浆蛋白电泳检查显示争产。超声,MRI和CT扫描检查各部位均显示正常。
图1:
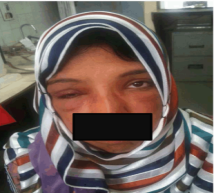
根据抗核抗体(ANA)阳性和低补体血症诊断为获得性血管性水肿伴潜在的免疫复合物病。患者C2补体1.3 mg/dL(正常范围1.6–3.5 mg/dL),C4补体8.2 mg/dL(正常范围10–50 mg/dL),C3补体82 mg/dL(正常范围90–180 mg/dL)。
考虑到双血球减少,淋巴细胞减少,ANA阳性,低补体血症,怀疑系统性红斑狼疮。进一步检查发现抗双链DNA抗体(dsDNA)189 IU/L(正常水平<25 IU/L),狼疮性肾炎无临床症状(24h内尿蛋白 0.54 g/d), 患者拒绝肾活检,以上结果证实了系统性红斑狼疮。抗甲状腺过氧化物酶(TPO)抗体71.07 IU/mL(正常范围<35 IU/mL),进一步表明与自身免疫性疾病有关。
在门诊处,患者接受口服糖皮质激素中等剂量0.5 mg/k,持续6周,之后保持0.07 mg/kg/d。现在患者状况良好,无蛋白尿,全血细胞计数(CBC)正常,外观改善。在接受治疗的第6天,患者血管神经性水肿症状减轻。随访时C1-INH水平和C4补体水平恢复正常,分别为224 mg/L和13 mg/dL,最近一次随访时分别升至310 mg/L和48 mg/dL。最近一次检测时,抗TPO抗体降至正常范围。患者一直在我院变态反应科/免疫科规律随访。
讨论
获得性血管性水肿最初发作人群为40岁及以上、出现复发性皮肤和/或粘膜血管性水肿、无荨麻疹的患者。该病可无明显的诱因,无家族病史。对于该病患者,应先检测其C1-INH和C4抗原。本例患者C1-INH水平较低,C3补体水平82mg/dL,C4补体8.2 mg/dL,提示获得性血管性水肿伴潜在的变态反应性疾病。狼疮患者出现获得性血管性水肿与经典途径介导的低补体血症(C3和C4水平较低)和短暂的C1-INH水平较低和功能较低有关。狼疮患者出现AAE还与淋巴组织增生性疾病缺乏和临床SLE活性缺乏有关。
由于患者出现了急性血管性水肿,我们主要考虑了变态反应性疾病,没有考虑系统性红斑狼疮。为了确诊,额外检查淋巴组织增生和自身免疫性疾病,包括CBC、ESR、抗核抗体、抗TPO抗体、24h内尿蛋白、骨髓检查和全身扫描。由于患者无热,眼眶MRI检查显示正常,所以眼眶蜂窝织炎和假瘤可能性较小。患者无淋巴组织增生性疾病(如眼眶非霍奇金淋巴瘤),影像学检查和骨髓检查排除毛细胞白血病。虽然淋巴组织增生性疾病常见于AAE,二者间有直接的发病关系。但也有报道称SLE、各类肿瘤和感染与AAE有关。良性淋巴组织增生性疾病,如意义不明的单克隆丙球蛋白病(MGUS),常常与AAE有关。患者血管神经性水肿症状于口服糖皮质激素治疗6天后减轻。免疫抑制疗法治疗后,C3、C4和C1-INH水平恢复正常,血管性水肿消失。
结论
过敏性血管神经性水肿继发于系统性红斑狼疮是由于获得性C1-INH缺陷、抗核抗体阳性、低补体血症。本病例表明,我们不应低估血管性水肿作为各种威胁生命的疾病的病因。
参考文献
1. Anthony S. Fauci et al. Principles of internal medicine. Harrison's. 2008 (17th Ed.); chapter 311; 2061–74.
2. Van Dallen RG, Maddox DE, Dutta EJ. Masqurades of angioedema and urticaria. Ann Allergy Asthma Immunol 2002;88(1):10–14.
3. Somani VK. Urticaria and Angioedema. In: Shaikh WA ed. Allergy and Asthma : A Tropical View. IJCP Publictions. Delhi 2001. pp. 231–48.
4. Hassan G, Khan GQ, Waseem Qureshi, Ibrahim M. Angioedema: Current Concepts. JK Science 2005;7(3).
5. Marco Cicardi, Andrea Zanichelli. Acquired angioedema. Allergy Asthma Clin Immunol 2010;6(1):14.
6. Manjari Lahiri, Anita YN Lim. Angioedema and systemic lupus erythematosus--a complementary association? Ann Acad Med Singapore 2007;36(2):142–5.
7. Nettis E, Colanardi MC, Loria MP, Vacca A. Acquired C1-inhibitor deficiency in a patient with systemic lupus erythematosus: a case report and review of the literature. Eur J Clin Invest 2005;35(12):781–4.
8. Nagy L, Hannema A, Swaak A. Acquired C1 inhibitor deficiency associated with systemic lupus erythematosus, secondary antiphospholipid syndrome and IgM monoclonal paraproteinaemia. Clin Rheumatol 1999;18(1):56–8.
9. Ochonisky S, Intrator L, Wechsler J, Revuz J, Bagot M. Acquired C1 inhibitor deficiency revealing systemic lupus erythematosus. Dermatology 1993;186(4):261–3.







