一例基底核区良性腺性神经鞘瘤病例分析
1.病历摘要
男,14岁;因“头晕、头痛,呕吐伴右侧肢体乏力7周,加重2周”于2012年10月入院。7周前病人出现头痛、头晕伴呕吐,当地医院MRI检查发现左侧基底核区占位并脑积水,行脑室-腹腔分流术,术后症状有所好转,2周前症状复发并加重。查体:右侧肢体肌力Ⅳ~Ⅴ级,左侧肢体肌力Ⅴ级,全身皮肤未发现牛奶咖啡斑、神经纤维瘤和听神经瘤等神经纤维瘤病症状,无神经纤维瘤家族史。
头颅MRI示:左侧基底核区占位,大小38mm×41mm×25mm,考虑血管性病变。术前诊断:①左侧基底节区占位;②脑室-腹腔分流术后40d。行体感诱发电位和运动诱发电位监测,显微镜下完整切除肿物。
标本送病理检查:病灶组织外观呈灰红、灰黄色,切面有出血点;镜下观察见肿瘤细胞呈长梭形,排列较疏松,在经典的神经鞘瘤背景即交替分布的AntoniA区和AntoniB区中散在分布腺样结构,被覆腺上皮和复层上皮,还可见肠腺上皮,并见少许退变的合体细胞样多核巨细胞;肿瘤内可见出血、坏死和囊性变,未见核分裂。
免疫组织化学示:梭形细胞S-100蛋白阳性,神经元特异性烯醇化酶(NSE)、细胞角蛋白(CK)、癌胚抗原(CEA)、嗜铬粒蛋白A(CgA)、胶质纤维酸性蛋白(GFAP)阴性;腺体结构CK、CEA阳性,S-100蛋白、NSE、CgA、GFAP阴性;两者Ki-67阳性率<1%。
病理诊断:良性腺性神经鞘瘤。术后病人症状好转,无神经功能障碍。术后34个月复查MRI未见肿瘤复发。
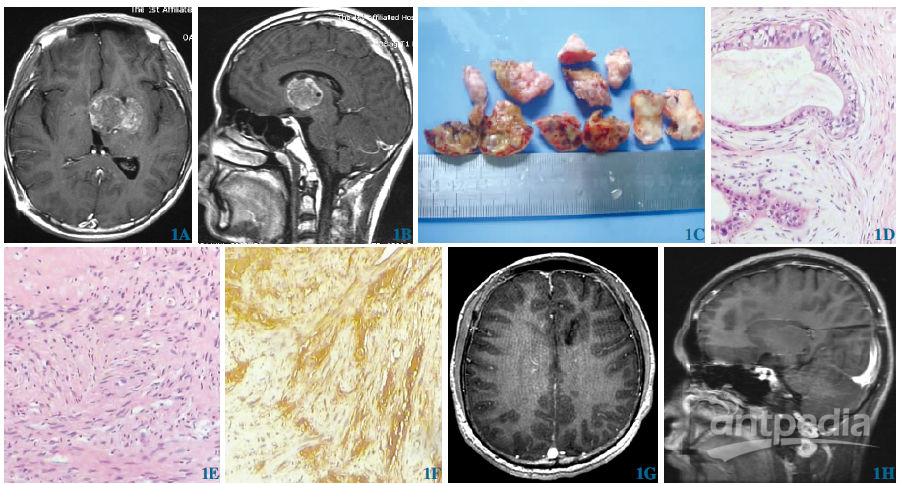
图1显微外科手术切除基底核区良性腺性神经鞘瘤。1A~1B术前MRI,考虑血管病变;1C标本外观;1D大小不等的腺样结构(苏木精-伊红染色×200);1E交替分布的AntoniA和AntoniB区(苏木精-伊红染色×100);1F梭形细胞S-100蛋白阳性,腺体阴性(免疫组织化学染色×400);1G~1H术后34个月MRI
2.讨论
腺性神经鞘瘤是神经鞘瘤的一种罕见类型,已报道病例多为恶性,且常伴神经纤维瘤病。良性腺性神经鞘瘤更罕见,通常进展缓慢,体积较小,直径多≤2.0 cm,以躯体、四肢多见。目前尚未见颅内良性腺性神经鞘瘤的报道。良性腺性神经鞘瘤的组织学特征为神经鞘瘤背景中出现腺体结构。
这种腺体结构的组织学来源仍有争议:Woodruff和Christensen认为是包埋的汗腺。本例腺体来源不是包埋的汗腺,因颅内没有汗腺,颅外的汗腺也不能迁移到颅内。Brooks和Draffen提出腺体可能是schwann细胞上皮化生。Ferry和Dickersin对假腺样神经鞘瘤的超微结构和免疫组化研究证实:排列在腺样空间里的细胞是schwann细胞,推测这种类型的schwann细胞可以提供普通schwann细胞和腺性神经鞘瘤之间的“过度细胞”。如果腺体结构是来源于schwann细胞的直接化生,那么“过度细胞”就会同时表达schwann细胞和腺体细胞的特征。但本例中并没有出现同时表达S-100和CK蛋白的过度区域,腺体结构也不是schwann细胞上皮化生。
也有学者提出腺性神经鞘瘤可能来源于多能神经嵴细胞,这是目前比较认可的假说。在个体发育中,神经嵴细胞可分化成多种结构,包括黑色素细胞、颅骨、几乎所有周围神经结构及其支持成分如神经胶质细胞和schwann细胞。这些部位发生的肿瘤有分化为腺瘤、黑色素瘤和神经鞘瘤的可能。
本例腺体结构可能来源于多能神经嵴细胞。目前为止,所有报道的良性腺性神经鞘瘤治疗效果均较好。但Chuang和Wang报道1例发生在胰腺后部的腺性神经鞘瘤,schwann细胞成分是良性的,而腺性成分显示异型性。良性腺性神经鞘瘤是否具有恶变可能,还需要长期随访。发生在颅内的良性腺性神经鞘瘤的术前诊断困难,需要与恶性腺性神经鞘瘤、双相滑膜肉瘤、假腺性神经鞘瘤及神经鞘瘤内的腺癌转移鉴别。治疗以手术切除为主,对放疗和化疗是否敏感,还没有相关报道。本例单纯手术切除治疗,术后34个月复查MRI未见肿瘤复发。肿瘤远期是否会复发,需要进一步随访。本例报告为良性腺性神经鞘瘤的发生部位和起源提供了更多可能。







