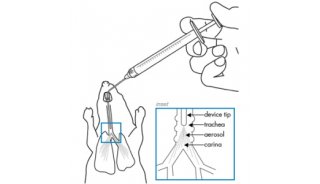
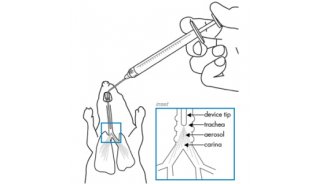
一例无形态学改变的肺内FDG高代谢结节PET/CT显像病例分析
患者男,58岁,因"发现肝硬化3年余,呕血伴昏迷20 d"入院。患者乙肝病史多年,3年前因肝硬化行脾脏切除,1年前曾因"肝性脑病"昏迷入院,20余天前自行停服抗病毒药物,2 d后出现意识不清伴呕血,再次入院,门诊以"肝性脑病"收住院。
住院期间查腹部增强CT:肝脏多结节灶,首先考虑肝癌;肝硬化,脾缺如,腹腔积液;胸部螺旋CT平扫:左下肺感染性病变,两侧胸腔积液。实验室检查(括号中为正常参考值):AFP 11.1(0.0~20.0) μg/L,CEA 7.0(0.0~5.0) μg/L,CA125 403.4(0.0~35.0) kU/L,铁蛋白1 505.3(7.0~323.0) μg/L;白细胞计数4.2×109/L[(4.0~10.0)×109/L],中性粒细胞百分比36.3%(50.0%~70.0%),单核细胞百分比22.9%(3%~10%)。
为明确肝内病变性质及评估全身情况行18F-FDG PET/CT(德国Siemens Biograph16)检查,结果示:肝硬化,肝右叶膈顶团片状FDG代谢增高灶,大小约2.9 cm×3.6 cm,SUVmax约3.4;右肺中叶结节状FDG代谢增高灶,延迟3 h、4.5 h显像FDG代谢仍增高,常规显像(注药后1 h)及2次延迟显像的SUVmax分别约23.4、23.2和24.1,CT上相应部位未见异常密度影(图1);PET/CT诊断:肝癌(高中分化可能);右肺中叶结节状FDG代谢增高灶,延迟3 h、4.5 h显像FDG代谢仍增高,建议结合CT增强密切随访。
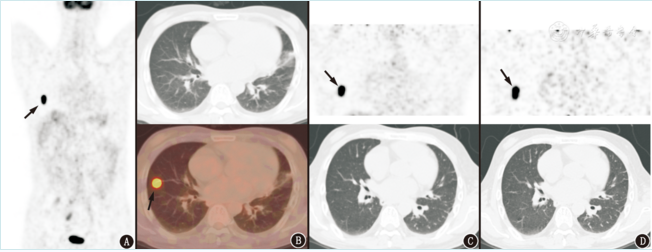
图1肝癌患者(男,58岁)18F-FDG PET/CT显像图(箭头示病灶)。A. MIP图,可见右肺局灶性高代谢病灶,SUVmax为23.4;B. CT横断位图像未见异常,PET/CT融合图像示右肺内高代谢灶;C.延迟3 h显像,MIP图可见右肺内局灶性高代谢病灶,SUVmax为23.2,CT横断面图像相应层面上肺内未见任何异常影像;D.延迟4.5 h显像,PET图像上病灶SUVmax为24.1,CT图像仍未见异常
患者肝内病变经肝穿刺病理证实为肝细胞肝癌。PET图像上右肺中叶的病灶在CT图像上相应位置未见异常改变,2 mm CT薄层扫描肺内仍未见解剖学异常。8 d后患者再次行胸部18F-FDG PET/CT检查,结果示右肺中叶结节状高代谢病灶消失,相应部位CT仍无明显异常(图2)。后患者经治疗好转出院,至投稿前未再次行CT检查。

图2肝癌患者(男,58岁)首次18F-FDG检查后8 d的再次18F-FDG PET/CT显像图。冠状面、矢状面及横断面的PET/CT融合图像及胸部MIP图像示高代谢灶消失(十字交叉处)
讨论
正常的肺在PET图像上呈低度摄取。不管是恶性病变还是如炎性反应、结核、肉芽肿或结节病等良性病变造成的肺内18F-FDG浓聚,在CT图像上相应部位均可见形态学的改变。本病例只有PET图像上的结节状高代谢病灶,CT图像上无明显异常,实属罕见,国内鲜有类似的报道,国外有个案报道。大部分学者倾向于此类浓聚灶是微血管栓塞导致,部分学者认为其与肺微小血栓的炎性反应相关。
复习国内外文献报道及结合患者临床资料和影像表现,笔者推测引起本例PET/CT显像肺内灶此种表现的原因如下:首先,由于静脉注射可以引起血管内皮的损伤,血管内皮损伤部位血小板可以被激活,引起血小板聚集、黏附,从而形成血栓。血小板的主要成分为细胞膜上的糖蛋白,细胞膜上的Glut3能介导血小板的黏附,在葡萄糖代谢的过程中能增加葡萄糖摄取,因此会造成栓子上的高18F-FDG浓聚。其次,带有18F-FDG的栓子通过体循环栓塞于肺内的小毛细血管里,造成肺内的高浓聚灶。Caobelli等也报道过静脉注射可引起肺内小血管的栓塞。还有学者报道微栓塞形成后肺内的小血管受伤,中性粒细胞被激活,中性粒细胞膜上的Glut1转运增强,从而引起葡萄糖摄取增高。由于肺内微小栓子体积小,CT扫描在相应部位无法显示形态异常。
本例患者在1周后的复查中,PET图像上高代谢灶消失,CT图像上肺内仍未见明显异常。本案例的不足之处是由于患者病情较重,不能配合次日局部18F-FDG PET/CT复查,未能及时对比。