一例发作性左上肢麻木及无力病例分析
患者男性,72岁,右利手。2014年11月6日因“发作性左上肢麻木及无力1周”入院。患者入院前1周休息时出现左上肢麻木不适,麻木感从左上肢远端向近端过电样蔓延至肩部停止,同时出现左侧肩胛区麻木不适,约1min缓解,麻木消失10min后出现左侧肢体无力,表现为上肢抬举困难,下肢沉重感,行走无力,20min后缓解。上述症状共发作3次。
既往史:左肾癌病史4年,于外院行手术治疗;高血压病史1年,未规律服药,血压波动在(130~150)/(70〜89)mmHg(1mmHg=0.133kPa)。
神经系统体检:无阳性体征。
辅助检查:心电图、心脏彩超、TCD、24h视频脑电图未见异常,血沉、风湿免疫系列、C反应蛋白(CRP)、血常规、尿常规、便常规、血脂、血凝均正常。
入院当日头部CT示:右侧额叶脑沟内条形稍高密度影,蛛网膜下腔出血可能性大(图1A)。次日头部MRI T1WI、T2W1示:(1)右顶叶脑沟内异常信号,考虑少许蛛网膜下腔出血可能性大(图1B、1C);(2)DWI序列示右侧枕叶新发腔隙性脑梗死(图1D)(3)横窦、乙状窦、直窦、上矢状窦未见异常,1周后(2014年11月13日)DSA示:颅内血管未见异常。
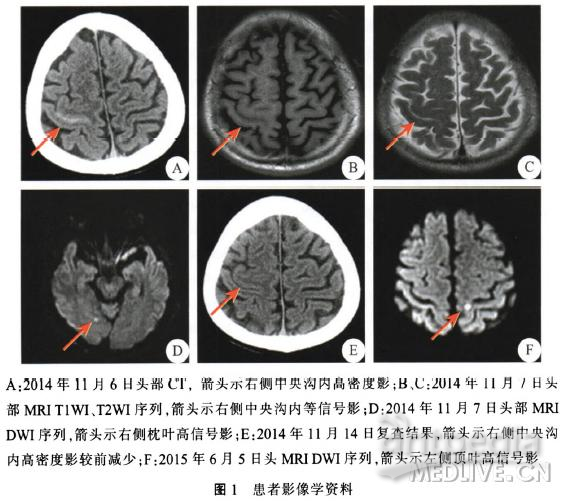
诊断:(1)凸面蛛网膜下腔出血(convexal subarachnoid hemorrhage,cSAH);(2)急性脑梗死。
治疗:嘱绝对卧床,给予营养神经及尼莫地平口服等治疗,同时监测血压。2014年11月14日复查头部CT示较前出血有所吸收(图1E),出院。出院后随诊,1个月内未出现左上肢麻木及无力发作,于2014年12月8日复查头部CT未见异常。
2015年6月2日患者以“发作性右侧肢体无力1d”为主诉再次入院,主要表现为右上肢突发无力,持物不能,持续约20min后缓解,共发作2次。头部CT示未见异常。2015年6月5日头部MRI示:左侧顶叶内新发脑梗死(图1F);MRA未见颅内血管异常。诊断:急性脑梗死。治疗好转后出院,随访至今,患者未再出现上述症状。
讨论
cSAH是非动脉瘤性SAH的重要亚型,其特点是出血局限在1个或几个大脑半球凸面皮质沟内,而不累及邻近的脑实质、大脑纵裂、基底池或脑室。常见病因是脑淀粉样血管病(cerebral amyloid angiopathy,CAA)、可逆性脑血管收缩综合征(reversible cerebral vasoconstriction syndrome,RCVS)、脑静脉血栓形成(cerebral venous thrombosis,CVT)、颈内动脉(internal carotid artery,ICA)狭窄/闭塞、可逆性后部白质脑病综合征(posterior reversible leukoencephalopathy syndrome,PRES)。常见症状为不同程度的头痛、癲痫、短暂性脑缺血发作(TIA)及局限性神经功能缺损症状。cSAH的诊断主要依据典型的影像表现:大脑皮质或相邻几个脑沟内线样出血信号,集中于单侧中央沟(80%〜90%)及中央前沟、顶内沟。
Kumar等总结29例cSAH,发现小于等于60岁组最常见的病因为RCVS,多以突发剧烈的头痛起病;而大于60岁组最常见的病因为CAA,通常以短暂的感觉或运动症状起病。周立新等报道8例cSAH,其中6例表现为发作性单侧肢体或面部抽搐,其中皮层静脉血栓2例、静脉窦血栓1例、CAA1例、血管炎1例。老年人(特别是无高血压病史者)cSAH病因则可能多为CAA,因淀粉样变性的血管主要位于脑沟和脑回表面的软脑膜血管,逐渐累及皮质血管。具体机制为β淀粉样蛋白(amyloid β-protein,Aβ)沉积于大脑皮层、皮层下及软脑膜中、小血管的中外膜,血管中层的平滑肌细胞被Aβ替代,血管弹力层破裂或破坏,最终导致血管纤维蛋白样坏死、微血管扩张、微动脉瘤形成、血管狭窄和血管破裂等病理改变;其次Aβ毒性作用也可导致皮质动脉血管反应能力受损进而使脑白质损伤。
本例患者高血压病1级,平素未口服降压药物,血压波动于(130~150)/(70~89)mmHg,本次颅内出血部位为靠近皮层且位于脑沟内,非高血压病性脑出血常见部位,高血压所致cSAH的可能性不大。患者头MRV及血清学检査正常,故除外CVT、血管炎、凝血机制障碍等所致cSAH。患者老年,发病时无头痛主诉,DSA检查未见异常,除外RCVS、颅内动脉瘤、血管畸形、动脉夹层等所致cSAH。患者脑出血合并反复脑梗死要注意颈动脉狭窄所致cSAH,但DSA检测结果正常,不符合ICA狭窄/闭塞所致cSAH特点。患者心脏彩超及DSA、TCD等检查正常,除外心源性、动脉源性栓子脱落所致反复脑梗死。患者反复脑梗死,部位主要位于皮层,病灶较小,合并脑出血,考虑与CAA相关,结合波士顿淀粉样脑血管病诊断标准及Linn等、Viswanathan和Greenberg的报道,考虑CAA可能性大。Viswanathan和Greenberg在对老年人血管淀粉样变研究中提出皮层微梗死是CAA所致脑梗死特点,这些微梗死灶可能与Aβ作用于脑血管致脑血流量异常调节有关,其中包括血管平滑肌变性及微血管梗死。有研究显示在CAA患者中存在DWI序列微缺血病灶占的15%,这些研究在神经影像学及梗死灶的神经病理学上显示病灶的大小、位置、特征与CAA高度相关性。头MRI的SWI序列可早期发现皮质下多发性微出血灶,为确定CAA病因诊断提供依据。但患者未行SWI,确诊尚需进一步行神经病理学检查。
CAA致cSAH的临床表现主要为反复性和多灶性的自发性颅内出血及认知功能障碍,另一临床表现为短暂性局灶性神经功能障碍发作,以反复、刻板发作为主,持续数分钟后缓解。后者分为阳性及阴性症状:阳性症状包括有先兆的扩散性感觉异常、视觉刺激症状或肢体抽搐,以感觉异常最常见,单肢及口周受累;阴性症状包括TIA、言语障碍、突发肢体无力及视力下降。近年来,短暂性神经功能障碍事件(transient focal neurological episodes,TFNE)在CAA中受到关注,这类事件在CAA较常见,表现类似TIA。其出现类似TIA症状可能与出血更相关,机制有人认为是由cSAH以及大脑皮质表面铁沉积引起。因此,TFNE可能是CAA症状性脑出血的早期高危预示因素。本例患者症状主要为发作性的左上肢麻木之后出现左侧肢体无力,左上肢发作性麻木类似癲痫,左侧肢体无力症状类似TIA。患者出现类似感觉性癫痫发作">癫痫发作,但行视频脑电图未见异常,考虑可能是发作间歇期行该项检查阳性率低;另外因出血量少,致痫灶本身局限性均可导致阴性结果。分析患者出现上述症状的机制可能为出血刺激皮层致癲痫发作,癫痫引起相应部位缺血缺氧导致血管痉挛,随之出现类似TIA表现,但尚需进一步病例研究探讨其可能的神经病理生理学机制。
目前鉴别老年患者血流动力学改变所致的cSAH和CAA所致的cSAH存在困难。前者血管狭窄引起慢性低灌注致动脉远端缺血缺氧,可引起血管新生及侧支血管形成,如果存在侧支血流代偿,可能在灌注成像上观察到相应皮层脑血容量增高、脑血流量正常、平均通过时间和达峰时间延长等影像学改变。而CAA所致cSAH不具有这些特点。
因cSAH存在多种病因,其治疗应根据不同病因进行,包括钙离子拮抗剂、抗癲痫药物,颈内动脉狭窄者可给予抗血小板和他汀类药物,符合手术指征者可行颈动脉内膜剥脱术等。因临床病例数较少,评估对症治疗的疗效仍需相应样本的病例研究。




















