完全型雄激素不敏感综合征病例报告
1 病例报告
患者,22 岁,因发现腹股沟包块 10 年,原发性闭经,于 2016 年 6 月 19 日就诊于我院。社会性别女,2006 年 4 月发现 双侧腹股沟区包块,无疼痛及增大,未重视。2010 年因无月经 初潮发现先天性无子宫。2014 年行染色体核型分析">染色体核型分析发现为 46,XY,未进一步诊治。21 岁结婚,婚后性生活正常。患者父 母非近亲结婚,家族中未发现其他人患此病。本次患者要求切 除腹股沟包块入我院。入院查体:女性体态,身高170 cm,无喉 结,乳房发育 T3 型(乳房、乳晕增大,两者呈一个小丘状隆起, 乳晕色素增生),无腋毛,外阴幼稚型,无阴毛,阴蒂略增大,尿 道开口于阴道外口上方,阴道呈盲端,深约 6 cm,未及宫颈、子 宫及双侧附件。左侧腹股沟区可及大小约 6 cm×4 cm包块,右 侧可及大小约 5 cm×4 cm 包块,质软,实性,边界清,活动可,无 压痛。实验室检查:卵泡刺激素(FSH)33. 83 U/L,黄体生成激 素(LH)34. 36 U/L,催乳激素(PRL)0. 36 nmol/L,孕酮(P) 1. 08 nmol/L,睾酮(T)11. 17 nmol/L,雌二醇(E2)7. 36 pmol/L。 彩超检查提示:盆腔积液(盆腔可见范围约4. 1 cm×2. 1 cm 无 回声区),左右腹股沟上方皮下分别可见 4. 8 cm×1. 4 cm、4. 4 cm×1. 6 cm 偏低回声(不排除睾丸组织结构可能),边界清,形 态规则,内回声不均匀,其内分别可见较多低回声小结节,左侧 较大结节约0. 5 cm×0. 4 cm,右侧较大结节约 4. 0 cm×3. 0 cm。 进一步行盆腔增强 CT 检查提示:子宫及双侧附件未见明确显 示;双侧腹股沟见结节影,增强扫描呈明显延迟强化,考虑双侧 腹股沟疝,隐睾可能性大,见图 1。术前诊断为完全型雄激素 不敏感综合征。于 2016 年 6 月 29 日在全身麻醉下行腹腔镜 探查术+双侧腹股沟包块切除术,术中探查见:子宫、输卵管、卵 巢缺如。盆腔积液较多,双侧腹股沟包块位于腹腔外,遂改开 放手术。先处理右侧腹股沟包块,依次切开皮肤和皮下组织, 切开腹外斜肌腱膜、腹横筋膜,牵拉出包块组织,约 4. 0 cm× 3. 0 cm×4. 0 cm,打开鞘膜,见类似睾丸组织,见图 2,充分游离 后离断缝扎,彻底止血,检查无误,依次关闭切口。同法处理左 侧腹股沟包块。手术顺利,术中出血约 5 ml。肉眼可见包块表 面囊泡数枚,直径 0. 5~ 1. 2 cm,内为清亮液体,切开可见一大 小约 3. 0 cm×2. 0 cm×1. 8 cm 的灰黄结节,实性,质韧,边界清, 其余切面灰白,实性,质韧,大小 4. 0 cm×2. 0 cm×1. 8 cm。术 后病理检查为:睾丸组织,发育不全的附睾及输精管组织,见图 3。术后第 6 天复查性激素:FSH 96. 01 U/L,LH 47. 53 U/L, PRL 0. 74 nmol/L,P 0. 41 nmol/L,T 0. 38 nmol/L,E2 < 1. 36 pmol/L。术后每日服用戊酸雌二醇片(商品名:补佳乐) 1 mg。出院诊断:完全型雄激素不敏感综合征。术后恢复好, 现随访中。

图 1 盆腔 CT 增强检查提示双侧腹股沟结节影,隐睾可能性大
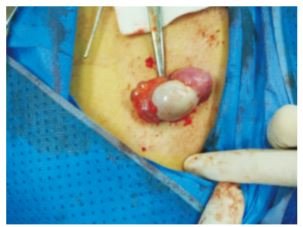
图 2 右侧腹股沟结节
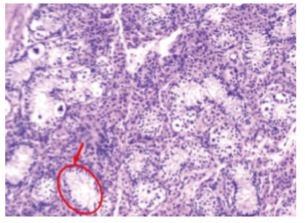
图 3 病理检查可见数个发育不全的曲精小管 (HE×200)
2 讨 论
雄激素不敏感综合征(androgen insensitivity syndrome,AIS) 是男性假两性畸形的一种类型,临床罕见。
2. 1 雄激素不敏感综合征的病因
本病最早于 1802 年 Tonin 等描述为“有睾丸的女性”。目前认为是位于染色体 Xq11-12 的雄激素受体(AR)基因突变引起的 X 连锁隐形遗传病,发病 率约为 1. 6/10 万~5. 0/10 万[1],显著特征为性分化异常。AR 异常导致雄激素的正常效应全部或部分丧失,根据患者临床有 无男性化表现,将 AIS 分为有男性化表现的不完全型 AIS(IAIS)和无男性化表现的完全型 AIS(CAIS)。CAIS 在男性新生儿中的发病率约为 1/20000~1/64000[2]。IAIS 患者可有不 同程度男性化表现,部分患者可有生育能力。本例属于 CAIS。
2. 2 CAIS 的诊断与鉴别诊断
此类患者的诊断主要是通过 临床表现、染色体核型分析、性激素测定及性腺病理检查等手 段。CAIS 通常以女性表现、原发性闭经为特征[3]。其个体体 型及外生殖器为女型,盲端阴道,子宫、输卵管缺如[4],可见青 春期乳房发育,但阴毛和腋毛稀少或缺如[5],染色体核型为 46,XY,性腺为睾丸,均无生育能力。睾丸位于盆腹腔、腹股沟 管或大阴唇内。目前已知国内最早有文献报道的为北京协和 医院,在其回顾性研究中提到,1984 年 6 月至 2009 年 3 月北京 协和医院共收治了 48 例 CAIS,收治了 26 例 IAIS,病理结果显 示性腺均为发育不全的睾丸,以腹股沟和盆腔内常见,大阴唇 内亦不少见[6]。 此类患者应与 46,XY 单纯性性腺发育不全及 46,XY 17 α 羟化酶缺乏相鉴别。这三类患者染色体均为 46,XY,外生殖器 均为女性,但由于病因不同,临床表现有所差别。46,XY 单纯 性性腺发育不全患者乳房不发育,有阴道和子宫,人工周期有 撤退性出血,性腺为条索样。而 17α 羟化酶缺乏的患者无乳房 发育,阴道呈盲端,人工周期无反应,常伴有高血压、低血钾、血 清 17 羟孕酮显著升高、尿 17 酮类固醇排出量增多等表现。 2. 3 CAIS 的早期诊断 AIS 遗传倾向明显,应重视产前诊断 。 有学者提出产前诊断时对有家族史者、高龄孕妇、有遗传病史 或有高危妊娠因素的孕妇,应进行羊水穿刺,确定胎儿性别为 46,XY 而 B 超检查发现外生殖器为女性表型时,应高度警惕 CAIS 的存在,并做进一步的检查,通过此方法最早可在孕 1 6 周发现 AIS[7]。因本病在临床上报道不多见,早期诊断存在一 定难度。但随着人们对该疾病的进一步认识,在新生儿时期 , 注意检查腹股沟和大阴唇内的包块,结合染色体的检查,可以 早期发现 CAIS 患者。而绝大部分的患者是在青春期后因原发 性闭经就诊,或伴腹股沟包块就诊,本例患者亦如此。 2. 4 AIS 的治疗 发育不全或位置异常的睾丸容易发生肿瘤 已成为国内外的共识,CAIS 中长期升高的 LH 可刺激睾丸的间 质细胞增生进而发生肿瘤[8],恶变的发生率随年龄增长而增 加, 20 岁时发生恶变率为 3% ~5%,50 岁时可达 50%[9],故手 术是治疗的主要手段,确诊后尽早手术切除睾丸[10],同时维持 女性特征,解决性生活问题。治疗的长期目标是,尽可能在外 观和功能上形成女性表现。在 CAIS 患者中,因其女性化程度 高,无男性化表现,只需切除双侧睾丸与疝修补术即可按女性 生活,IAIS 需根据外生殖器的畸形程度决定性别的选择。按女 性生活的 IAIS 需切除双侧睾丸,必要时行外阴整形或阴道成 形术。按男性生活的 IAIS 则需行隐睾纠正和外生殖器整形。 关于手术的最佳时间尚存争议。一种观点认为,婴儿期切 除睾丸可以防止睾丸肿瘤的发生,此时患儿没有对性别的认 知,减少了周围社会环境的影响,但是必须进行激素替代治疗 , 一般从 11 岁开始;而另一种观点认为,手术应该在青春期后进 行,这可以使患者在自身睾酮及雌激素的刺激下,在适龄期完 成身高及女性性征的发育,之后再改用雌激素替代治疗[11] 。 目前,并无两种手术时机对照研究的相关报道。手术方式可根 据性腺的位置来确定,术式有开腹或腹腔镜手术、经会阴切除术[6]。本例患者就诊时已经成年,第二性征发育及性心理已成 熟,术后病理检查未见恶变,术后恢复好,现随访中。
不管手术方式及时机选择在何时,术后均应长期服用雌激 素替代治疗,雌激素有助于诱导青春期,维持女性第二性征,完 善骨质生长,促进身心健康,防止因性激素缺乏引起并发症。 本例患者术后长期服用雌激素药物治疗。患者雌激素替代疗 法的最佳剂量尚未明确,目前往往依赖于个别专家的经验[12]。
人体骨密度可随年龄增加和雌激素下降而逐渐降低,无论 是 CAIS 还是 IAIS 患者性腺切除后,均会引起骨密度降低。有 研究报道,术后患者单纯的补充雌激素及增加雌激素的剂量, 均不能明显增加骨密度。说明雌激素和雄激素在骨量的获得 和维持的过程中缺一不可[13]。因此术后应用雌激素的同时加 用阿伦磷酸钠,理论上可以改善骨密度、防止骨量下降,预防骨 质疏松及骨折的发生。
参考文献略。







