一例胸椎管内脊膜瘤完全钙化病例分析
脊膜瘤是一种发生于椎管内的良性肿瘤,多起源于内皮细胞或纤维细胞,其发病率仅次于神经源性肿瘤,约占椎管内肿瘤的25%。主要发生于40~70岁的女性,其中约75%~83%发生在胸椎,女性∶男性为5.8∶1。脊膜瘤对放化疗等不敏感,通常需要手术完整切除肿瘤,预后满意,复发率低。大部分脊膜瘤为硬膜下髓外占位性病变,极小部分生长于硬膜外,肿瘤与硬膜关联紧密。钙化发生率约占椎管内脊膜瘤的1%~5%,但脊膜瘤完全钙化国内外鲜有报告,我院2016年3月收治1例T7节段脊膜瘤完全钙化患者,手术治疗后取得了良好效果,报告如下。
临床资料
患者女,57岁。因行走不稳伴不自觉摔倒1年半,就诊于外院诊断为“腰椎管狭窄症”,给予理疗、按摩,症状无明显好转。8个月前出现胸背部疼痛及右下肢麻木,逐渐发展至脐水平,在外院诊断为“胆囊炎”、“腰椎管狭窄症”,给予对症治疗后胸背部疼痛缓解,余症状无改善,并开始伴有大小便功能障碍,入院前1个月加重。
查体:脊柱无畸形,胸背部局部轻度叩击痛,无压痛,四肢肌张力不高,脐以下浅躯干感觉减退,双下肢浅感觉减退,左侧为重,本体感觉存在,右侧鞍区感觉减退。髂腰肌肌力右侧2级,左侧3-级,双侧股二头肌肌力4-级,其余肌肉肌力正常。双侧膝腱反射亢进,双侧跟腱反射活跃,腹壁反射存在,右侧肛门收缩反射减退,双侧Babinski征(+)。JOA评分5分(11分法)。
辅助检查:脊柱X线片示生理曲度存在,未见明显骨质破坏及增生。胸椎MRI示T7水平椎管内占位,为等长T1短T2信号,压脂像呈混杂稍高信号影,肿物明显压迫脊髓,脊髓受压变扁,脊髓内可见水肿信号(图1、2)。胸椎CT示T7水平椎管内可见团状高密度影,偏右侧,边界清,冠状位见高密度肿物,约2.5×1.5CM(图3~5)。结合相关检查及查体,诊断为胸椎椎管内占位性病变,性质等查。以“胸椎管内占位性病变”收入我院,拟行手术探查。完善术前准备后,在全麻下行后入路胸椎椎管内肿物切除减压植骨融合内固定术。
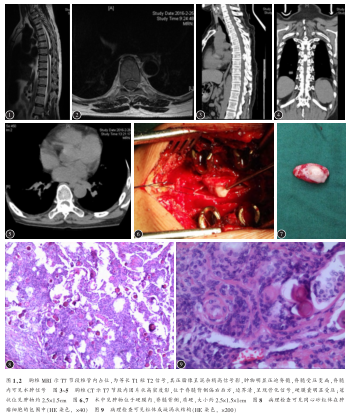
患者俯卧位,显露手术节段后,于T7、T8双侧置入4枚椎弓根螺钉,用磨钻磨除椎板,掀开椎板后见T7水平椎管内黄韧带无明显增厚,硬脊膜向后膨隆,无明显搏动,椎管后方硬膜触之较硬,沿硬膜中央切开硬脊膜,见一约2.5×1.5×1CM椭圆形肿物(图6),质地坚硬,表面不光滑,无包膜,基底乳白色、质韧(图7),内无明显神经行走,用神经剥离子小心分离肿物,肿物与周围组织无明显粘连,切除肿物后,见硬膜完整,脊髓无损伤,彻底止血后用无损伤线连续缝合硬膜,缝合后无明显脑脊液漏出,硬膜搏动良好,以适当大小硬膜补片修补硬膜囊,外敷明胶海绵,于T7、8双侧关节突间行植骨融合,逐层缝合切口。
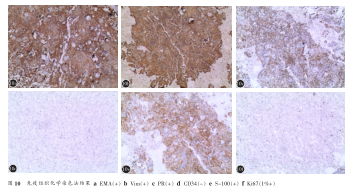
病理学报告:脊膜瘤钙化,可见砂粒体,内皮细胞型WHOⅠ级(图8、9)。免疫组化:EMA(+),Vim(+),PR(+),CD34(-),S-100(+),Ki67(1%+)(图10)。术后第1天自述下肢麻木及肌力较术前明显改善,髂腰肌肌力双侧4级,下肢活动灵活。术后2周JOA评分11分。佩戴胸部支具下地行走正常,未感觉行走不稳,双下肢腱反射仍活跃,右侧鞍区及双下肢无明显感觉减退,未查及明显感觉平面,大小便功能恢复正常,双侧Babinski征(+)。术后3个月复查CT示胸椎内固定物位置良好,无松动,植骨确切,已融合。双侧膝腱反射仍活跃,双侧跟腱反射正常引出,双侧巴氏征(+)。
讨论
根据WHO神经系统肿瘤分类(2016年),脊膜瘤可分为内皮型、纤维型、砂砾型、过渡型、分泌型等15个类型,其中以前三种最为多见。但脊膜瘤发生钙化较少见。
Alafaci等回顾国内外文献报道脊膜瘤完全钙化病例22例。钙化常常出现在沙砾型和内皮型中,钙化很少能达到接近骨化的程度,因一般含水量仍较高,血供丰富。此例患者瘤体背部呈完全钙化,CT显示为高密度影,发生几率极小。脊膜瘤患者未出现脊髓功能损伤及神经功能障碍前多无明显症状,常以胸背部疼痛为主。Engelhard等报道患者疼痛发生率约为52.2%,其胸背部疼痛易被误诊,从而延误治疗。本例患者于8个月前出现胸背部疼痛误诊为胆囊炎,经对症治疗后疼痛缓解。疾病早期无明显症状时,X线片的发现率低,不易确诊。
本例患者因病变位于硬膜内脊髓背侧,瘤体背部完全钙化,术前CT、MRI示肿瘤呈现广基底,与硬膜及椎板无明显界限,病灶表面不光滑,瘤体钙化占据椎管大部分空间,脊髓受压明显,压迫最重水平未见脑脊液信号,且矢状位影像学瘤体钙化影像与黄韧带关联紧密。故易误诊为黄韧带骨化症或硬膜外肿瘤,从而影响手术方案的设计及术前准备。
分析易误诊原因如下:(1)肿瘤信号少见。一般脊膜瘤无完全钙化表现,CT平扫为实质性,密度常稍高于正常脊髓,MRIT1加权像多呈等信号或稍低信号,信号比较均质,T2加权像肿瘤信号常稍高于脊髓。本例患者可见肿瘤背部完全钙化,CT示T7水平椎管内一团片状密度增高影,位于椎管后方,与椎板及黄韧带关联紧密;MRI成等长T1短T2信号影,压脂呈混杂稍高信号影,T2加权像低信号为骨化表现。(2)肿瘤生长方式少见。椎管内肿瘤根据病变所发生部位可分为髓内肿瘤、髓外硬膜内肿瘤及硬膜外肿瘤。髓内肿瘤病变区脊髓呈梭形肿胀,两侧蛛网膜下腔均匀变窄。髓外硬膜内肿瘤常与脊髓夹角为锐角,压迫脊髓移位,病侧蛛网膜下腔扩大,健侧变窄。硬膜外肿瘤常为梭形,病变邻近硬膜下腔呈“鼻尖样”狭窄,病变内侧可见受压移位的低信号硬脊膜影,脊髓受压推移。因此蛛网膜下腔是否增宽为鉴别椎管内肿瘤位于硬膜内还是硬膜外的一个重要依据。脊膜瘤常于髓外硬膜内生长,病变与一侧硬脊膜呈宽基底相连,包膜完整。术后回顾阅读MRI可见瘤体周围有完整硬脊膜影,因而术前仔细阅片可帮助明确肿物的位置及性质。
因脊膜瘤对放化疗不敏感,且手术复发率低,故手术为首选治疗方式。本例患者T7水平占位,因胸椎椎管小,为减少对脊髓的震荡和刺激,术中必须充分显露,不能采用骨凿等器械,应用磨钻或超声骨刀去除椎板。如肿瘤位于硬膜外,掀开椎板后,用神经剥离子探查周围组织,仔细分离瘤体后取出;如为髓外硬膜内肿瘤,则需用尖刀切开硬膜,一般以瘤体中央沿身体长轴切开,并用缝线牵引、固定硬膜,用神经剥离子探查肿瘤大小,确认与周围组织是否紧密粘连,确认与周围组织分离后完整取出瘤体。对于本例脊膜瘤伴钙化患者,沿中线切开硬膜,可见乳白色钙化瘤体占据整个椎管后侧,因与硬膜及蛛网膜无紧密粘连,完整分离瘤体与硬膜后,硬膜无缺损,给予缝合。若钙化瘤体与周围组织粘连紧密,在分离过程中需注意避免损伤脊髓造成术后症状加重。
Gezen等认为术中给予激素可减轻术后脊髓水肿。若与硬膜粘连无法分离,可一并切除后用人工硬膜修补,上覆明胶海绵。术后常规留置引流,给予糖皮质激素、脱水、预防感染、对症支持治疗,胸部保护性支具制动3个月。因患者术中需切开硬膜致脑脊液漏,故术后需给予能透过血脑屏障抗生素如头孢曲松预防感染。佩戴支具下地行走前,应于病床加强术后功能锻炼,预防因卧床导致的下肢静脉血栓形成。观察患者术后症状、体征等变化,包括胸背部疼痛,大小便功能的改变,鞍区及下肢感觉和下肢运动功能、腱反射和病理征的改变。术后3个月、6个月、1年影像学复查以了解肿瘤切除后脊柱脊髓情况、病变节段脊柱稳定性、内固定位置及植骨融合情况,并观察患者恢复情况。
总之,脊膜瘤完全钙化在临床上少见且易误诊,完善的术前准备可以减少治疗过程及手术过程中可能出现的困难,避免延长手术时间,并将术后如截瘫等并发症的风险降至最低。MRI可帮助诊断所有的脊膜瘤,并提供术前影像。但是MRI对分辨瘤体中的钙化不是特别敏感。未发现脊膜瘤钙化患者T1WI有典型的骨髓高信号影;术前CT对于制定手术方案,分辨瘤体中钙化部分的范围及大小至关重要。




















