一例腰椎管内副神经节瘤病例分析
副神经节瘤起源于神经嵴细胞,属于神经外胚叶肿瘤,是一类少见的神经内分泌肿瘤,目前公认的定义为:位于肾上腺髓质的副神经节瘤称为嗜铬细胞瘤,位于肾上腺外的副神经节瘤则依据解剖、功能状态或良恶性等综合因素命名,可发生于全身各部位,以头颈部(颈动脉体、颈静脉球、迷走神经内、甲状腺等)最为常见,发生于椎管内较为少见。本科诊治1例,报告如下。
临床资料
病例报告 患者,女,51岁,家庭主妇。因“腰部疼痛伴右下肢放射痛1年加重2个月”于2015年3月26日入院。患者1年前无明显诱因出现间断性腰痛并向右下肢放射,呈渐进性加重,以小腿外侧及足背为著,跛行。无既往病史。查体:体温36.8℃,脉搏65次/分,血压130/80mmHg(1mmHg=0.133kPa)。腰椎活动度减低,L4、5椎体棘突双侧压痛、叩击痛(+),双侧会阴部皮肤感觉减退,双侧直腿抬高试验60°(+),加强试验(+)。右侧足⻊母背伸肌力4级,余双下肢肌力正常。双侧膝腱反射减弱,双侧跟腱反射消失,双侧Hoffman征、Babinski征未引出。小便淋漓不尽,大便正常。影像学资料见图1。
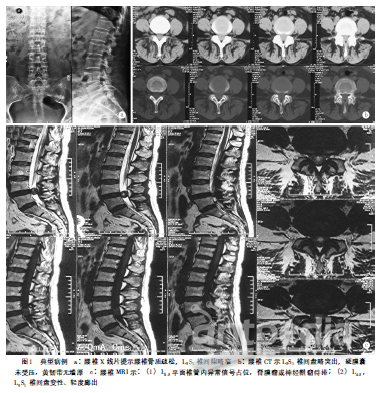
入院后治疗 入院后完善各项术前检查,在全麻下行“L4、5椎板切除减压、肿物切除、植骨融合内固定术”,切除L4椎板后可见L4、5节段硬膜囊饱满,打开硬膜后可见一大小约1.8CM×1.5CM×1.2CM大小肿物,包膜完整、暗红色、表面光滑、成多结节状,肿瘤背侧、腹侧浅表处与马尾神经粘连严重,部分神经纤维丝镶嵌于肿瘤中,肿瘤与硬膜囊之间界限清楚,仔细小心分离粘连,未离断神经终丝情况下完整去除肿瘤。仔细止血,缝合硬膜。常规L4、5节段安装内固定系统,放置引流管,逐层缝合。术后腰腿痛症状明显缓解,第7d康复出院。
病理检查 肿瘤切面灰红灰褐色,实性质软。镜下见梭圆形细胞排列成巢团状,腺样或乳头状,间质富含血管(图1d)。免疫组化结果:AE1/AE3(±),EMA(-),GFAP(-),S-100(局灶支持细胞+),CD56(+),Vim(+),PR(-),CgA(+),NSE(+),Syn(+),CD34(血管+),Ki-67增值指数<5%。病理诊断:副神经节瘤(图1e),局部细胞生长较活跃。
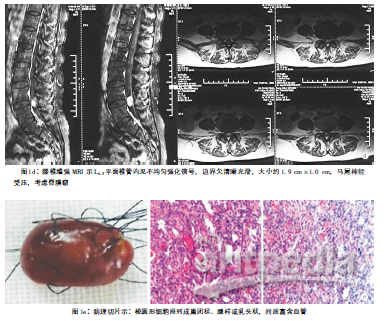
讨论
脊柱副神经节瘤是一种极为罕见的肿瘤,如果发生于椎管内,以马尾区多见,主要位于硬膜内髓外间室,肿瘤与终丝附着或粘连,少数发生于神经根。根据肿瘤能否分泌儿茶酚胺类物质,脊柱副神经节瘤分为功能性和非功能性副神经节瘤,绝大多数为后者,前者极为罕见。一般位于椎管内的副神经节瘤主要引起脊髓压迫症状,比如腰背痛及相应节段神经压迫症状,伴或不伴下肢运动或感觉功能障碍及膀胱和直肠功能障碍。如果肿瘤具有分泌儿茶酚胺类物质功能,除会产生脊髓受压症状外,还有高血压、潮汗、震颤、心动过速等症状。文献报道绝大多数原发于脊柱的副神经节瘤为无功能性。本例患者就诊时除脊髓受压症状外,无其他明显异常。
目前副神经节瘤病因不明,有学者认为本病与遗传因素有关。但本例患者无家族病史,临床症状无特异性,主要表现为脊髓神经的压迫症状。大部分无功能性脊柱副神经节瘤患者因神经压迫症状就诊时通过MRI发现椎管内占位性病变,其诊断主要依靠MRI发现椎管内占位性病变,同时也是术后复查的主要手段。本例患者腰椎X线片及CT扫描未发现明显占位病变。
脊柱副神经节瘤的MRI成像有一定的特点:肿瘤在T1WI像为低中信号,T2WI像为中高信号,由于富含血管,在缓慢血流和肿瘤本身形成的增强信号背景中,会出现圈点样空流区域,呈现葡行性条状低信号,即“椒盐征”,是其特征之一,但仍然难以与其他富含血管的肿瘤完全鉴别,如血管母细胞瘤、血管瘤等。同时应与神经鞘瘤、神经纤维瘤和脊膜瘤等相鉴别。本例术前核磁表现为等T1混杂T2信号占位,病灶中心可见斑片状长T2信号,影像报告考虑为脊膜瘤。而脊膜瘤是一种好发于胸段脊髓硬膜内或硬膜外的椎管内肿瘤,在T1WI呈低或者等信号影,T2WI呈稍高或等信号影,其特征与本例术前MRI平扫极为相似。MRI增强扫描也许能为两者鉴别诊断提供依据,副神经节瘤由于富含血管,常会出现“椒盐征”而脊膜瘤强化后可勾画出完整的轮廓肿瘤,且可见“脊膜尾征”。
还需与之鉴别的神经鞘瘤和神经纤维瘤常位于脊柱两旁,可单发和多发,青年、成人多见,多呈梭形或哑铃状,边界清楚,神经鞘瘤常伴有囊变坏死,平扫呈等或低密度,增强扫描实质部分强化明显,神经纤维瘤强化常不均匀且可伴有神经纤维瘤病,相邻椎间孔可扩大,二者强化程度均不及副神经节瘤。尽管脊柱副神经节瘤与其他脊柱肿瘤影像学表现各有一定的特点,但并不具有特异性,肿瘤类型的确诊只能通过组织病理及免疫组化染色,本例增强MRI扫描后瘤体仍为不均匀强化信号影,难以与其他肿瘤鉴别,最终确诊需依靠病理学。
脊柱副神经节瘤的大体病理表现为实性,部分或全部由包膜包绕,切面成红或褐色,易出血,可有局灶性纤维化。镜下主要由两种细胞构成,Ⅰ型主细胞和Ⅱ型支持细胞。Ⅰ型主细胞呈多边形、卵圆形、梭形,胞质丰富,淡红染或细颗粒状,细胞呈团状、巢片状排列或典型的“器官样”排列,间质富于毛细血管,支持细胞包绕主细胞,典型图像称为Zellballen细胞巢。偶尔可见出血,含铁血黄素或钙化,少见见数分裂和异型性。本例患者肿瘤组织切片具有非常典型的病理学表现。
免疫组化染色不仅可以对副神经节瘤特有细胞进行标记而且能反映其生化和内分泌功能,对确诊及其生物学特性的判断都非常重要。确定Ⅰ型主细胞最重要的神经内分泌标志物是嗜铬粒蛋白(CgA)、突触素(Syn)和神经元特异性烯醇酶(NSE);确定Ⅱ型支持细胞的是S-100蛋白或胶原酸性纤维蛋白(GFAP)阳性。神经内分泌标志物如CgA、Syn、S-100蛋白、NSE阳性及上皮源性标志物如CK、EMA等阴性有利于鉴别室管膜瘤、神经鞘瘤、脊膜瘤、脊索瘤等。
本例患者CgA、S-100蛋白、NSE(+)、Vim(+)免疫组化染色均为阳性。而Ki-67是反应细胞增殖活性的重要指标,与肿瘤的恶性程度、种植、转移、浸润相关,肿瘤组织中Ki-67阳性的细胞核越多,患者预后相对较差,在WHO的内分泌肿瘤组织学分类中,Ki-67指数<2%是肿瘤分化良好的标志。本例Ki-67增殖指数<5%。局部细胞生长较活跃,难以仅此判断良恶性,需要长期的随访观察。脊柱副神经节瘤大多数为良性,恶性少见,即使病理组织学也难以完全判定肿瘤的良恶性,诊断时应结合其生物学行为,如果肿瘤发生淋巴结转移和(或)远处转移,可认为是恶性副神经节瘤。
因此长期随访对于判定患者预后意义重大。手术完整、彻底的切除肿瘤是防止复发、提高生存率的关键。肿瘤能否完整切除,除对于患者预后至关重要。如不能完整切除,术后辅以放疗可有效缓解临床症状、提高远期生存率,而大多数学者认为化疗意义不大。







