胫腓骨大块骨溶解症病例分析
大块骨溶解症(MO),又称Gorham病、Gorham-Stout综合征、消失骨病、自发骨溶解症、幽灵骨病等,最早于1838年由Jackson率先报道,于1955年由Gorham和Stout整理相关个案资料对本病进行了系统描述,Johnson和Mcclure于1958年将本病正式命名为MO,现多采用此名。MO具有进行性骨溶解吸收的临床特点,临床上少见,全世界仅200余例报道,目前关于其病因、诊断、治疗等方面仍存较大争议,尤其缺乏长期随访结果评估疗效,且药物治疗后病灶骨溶解静止并出现骨化者尚未见报告。我院(深圳市第二人民医院)收治1例右胫腓骨远端MO患者,其病情进展迅速、治疗见效快、药物治疗后病灶静止并骨化、术后5年随访无复发,现报告如下。
病例资料
患者,男,36岁。2011年8月20日因扭伤致右踝肿痛,至当地医院就诊,行X线片检查(图1a)后诊断为“右胫骨撕脱性骨折”,予石膏固定、草药外敷治疗。因右外踝肿胀加重,伴夜间静息痛、右踝关节活动受限,于2011年10月28日转诊至我院。
查体:右外踝肿胀明显,局部皮肤呈暗红色,浅表静脉无曲张,皮肤无破溃,皮温增高,右小腿远端广泛肿胀,局部可触及质韧肿物,基底广泛,移动度差,肿物局部有压痛,无放射痛,右踝关节活动受限,右髋、右膝关节活动正常。实验室检查:WBC、ESR、中性粒细胞百分比、碱性磷酸酶、酸性磷酸酶等均正常,PPD试验阴性。X线片检查示右侧胫腓骨远端溶骨性病变,病灶范围较前明显扩大(图1b)。CT、MRI检查(图2)均提示右胫腓骨远端溶骨性破坏及周围软组织病变,右距骨、跟骨部分受累,考虑恶性肿瘤性病变所致。于2011年10月31日行右踝病灶穿刺活检术,术后病理结果:考虑血管外皮瘤可能,与影像学诊断不完全一致,肿瘤组织太少,必要时重新活检。
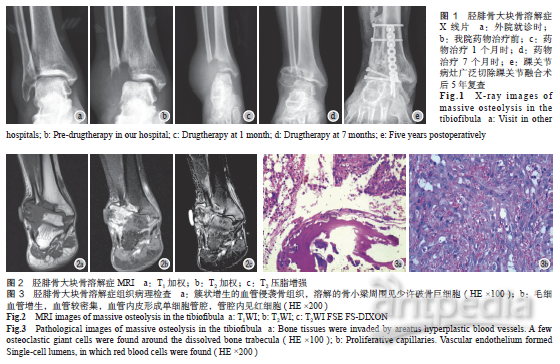
遂于2011年11月7日再次行右踝病灶穿刺活检,术后病理示:成簇大小不等增生的血管,血管间可见增生的纤维母细胞及硬化的胶原,部分似毛细血管,血管内皮细胞增生,少许呈乳头状伴有纤维素渗出;免疫组织化学检测示:增生的血管内皮CD34、CD31、FVIII阳性,小血管周围见SMA阳性的血管周细胞,HMB45阴性,Ki67<3%,成簇增生的小血管向骨组织内浸润性生长,局部区域见少许破骨细胞(图3)。综合临床、影像及病理学资料诊断为“右胫腓骨远端MO”。
明确诊断后,患者拒绝截肢,要求保肢治疗。建议患者行唑来膦酸联合钙剂及维生素D方案控制病灶,由于缺乏MO相关药物治疗剂量及疗程方面的研究,因此,经患者知情同意后予静脉滴注唑来膦酸抑制骨吸收治疗,每次给药4mg,给药间隔时间为28天,同时每日口服1片碳酸钙D3片(含600mg钙、125单位维生素D3),直至病灶稳定时,共应用唑来膦酸治疗7个周期。治疗期间患者病灶局部静息痛症状逐渐缓解,但负重活动仍痛性受限,及时复查血电解质、肾功能等检查,患者未出现发热、钙磷镁水平过低、肾功能损害、眼部炎症、颌骨坏死等不良反应及并发症。定期复查X线片,治疗1个月时见溶骨性病变静止(图1c),3个月时病灶范围开始缩小并出现骨化,7个月时病灶明显缩小并骨化(图1d)。病灶稳定后,为降低复发风险及重建患肢功能,于2012年7月9日行右踝关节病灶广泛切除踝关节融合术,术中见:右胫腓骨远端溶骨性病灶已完全硬化,边界清楚,剖面颜色呈暗红、灰白混杂,质硬。术后病理示:局部见纤维软骨化生及骨化,脱钙后见大量纤维组织增生、胶原化,少数小血管增生,考虑MO治疗后改变可能;免疫组织化学检测示:β-catenin(+),SMA(+),Ki67约1%(+),S100(-),CD34血管(+)。病理诊断为MO伴骨化。术后定期复查X线片,已随访5年余,右踝关节完全融合,病变无复发(图1e)。
讨论
病因 目前关于MO的病因主要有以下观点:(1)血管组织异常增生;(2)循环中PDGF-BB水平上升,通过相关信号通路促进淋巴管内皮细胞增殖;(3)淋巴管、血管畸形紊乱;(4)外伤致无症状性错构瘤激活;(5)局部缺氧和酸中毒引起酶水解;(6)破骨细胞前体对体液因子的敏感性增加,促进破骨细胞形成及骨吸收,此外单核巨噬细胞也参与骨吸收,其中白细胞介素-6、白细胞介素-1及肿瘤坏死因子等起重要作用;(7)局部成骨细胞活动受抑制。然而,尽管观点众多,但目前为止尚无一种理论能完全解释疾病过程。
诊断 虽然目前MO病因未明,但包括报告病例在内,不少案例在发病前有外伤史,提示外伤可能与MO起病有关联,明确的外伤史对诊断MO具有一定的参考价值。MO可发生于任何年龄,以青少年为主,好发于骨盆、肩胛骨、脊柱等部位,极少发生于胫腓骨远端,部分案例的病程具有自限性,其临床表现视发病部位不同而不同,最常表现为局部疼痛、肿胀及功能损害,或合并病理性骨折,但无特异性。实验室检查主要为排除其它疾病,如感染、结核、甲状旁腺机能亢进等。影像学检查方面,X线为主要检查手段,可见大量骨质溶解、消失,但无骨质增生硬化及骨膜反应,MO初期的X线征象易与骨质疏松所致骨量丢失相混淆,但随着骨皮质的溶解吸收,残端变细,后期呈“笔尖样”改变,直至骨完全溶解消失,而本案例的X线表现为典型的“笔尖样”改变,且这种溶解可延伸至直接关节以外,累及相邻骨。CT可见局部骨质破坏及软组织影。MRI检查中,骨质受累区域T1WI呈低信号,T2WI呈中、高信号。CT及MRI往往表现为恶性肿瘤征象,与临床表现及病理不一致,易致误诊、漏诊。本病例CT及MRI征象与文献报道相符,且从本病例MRI增强图像中可见病灶区域无明显强化,提示病变局部血供并不丰富,因此MRI增强图像可能有助于鉴别MO与血供丰富的恶性肿瘤。
MO误诊率很高,需综合临床、影像及病理学资料作出诊断,其中病理学依据具有确诊意义。Heffez等于1983年提出MO的8条诊断标准:(1)活检发现血管瘤样组织存在;(2)无细胞异型性;(3)无或仅有轻微成骨反应,无不良钙化;(4)有局部骨质进行性溶解吸收的证据;(5)非膨胀性、溃疡性病变;(6)无内脏受累;(7)影像学呈骨溶解征象;(8)无遗传、代谢、肿瘤、免疫及感染病史。鉴于近年有研究证实病灶内脉管为淋巴管,而非血管,因此诊断标准应相应作出调整。结合本病例,多次活检及获取足够样本量,有利于作出准确的病理诊断,必要时可考虑CT引导下穿刺活检或切开活检。MO的鉴别诊断包括遗传性多发骨溶解、肾病相关骨溶解、骨髓炎、类风湿性关节炎、骨内恶性肿瘤所致骨溶解、甲状旁腺机能亢进、嗜酸性肉芽肿以及中枢神经系统疾病所致骨溶解,如脊髓空洞症和脊髓痨等。
治疗 由于病因未明及发病率极低,MO尚无确切有效的治疗方案,目前对于MO的治疗原则是抑制骨吸收、预防和处理并发症,主要的治疗手段包括手术、放疗及药物治疗。手术主要用于病灶切除、功能重建及处理并发症,对于骨溶解进程未得到控制的病例,不宜进行功能重建手术,否则易致内固定失败。而放疗多被提倡用于病灶部位无法手术、病灶多发以及术后复发的病例,根治性治疗剂量推荐40~45Gy,而低剂量放疗可用于术前辅助控制局部骨溶解,尽管有研究对44例MO患者进行放疗,平均随访47.5个月其病灶控制率达到77.3%,但放疗可致骨坏死、肉瘤恶变、发育不良等严重并发症,因而限制了放疗的应用。药物治疗用于抑制骨吸收、稳定病灶,主要药物包括二磷酸盐、降钙素、干扰素以及成骨营养素(如钙、磷、维生素D)等。
目前主张综合治疗MO,本病例在病灶切除联合功能重建手术前先采用唑来膦酸、钙剂及维生素D联合方案抑制骨吸收治疗,经治后患者症状缓解,病灶局部骨溶解静止并明显骨化,提示该药物方案不仅可抑制病灶骨吸收,还具有局部成骨的作用。其中二膦酸盐的作用机制可能包括以下几点:(1)促进骨保护素的表达、降低巨噬细胞集落刺激因子的水平,从而抑制破骨细胞的生成;(2)通过抑制甲羟戊酸生物合成途径的关键酶-法呢基焦磷酸合酶的活性影响破骨作用;(3)二磷酸盐的AppCp类型代谢物与细胞毒性有关,可促进破骨细胞凋亡;(4)通过诱导糖皮质激素的代谢以及依赖联接蛋白43通道的开放发挥抗骨细胞及成骨细胞凋亡作用等。钙剂、维生素D则可为成骨活动提供原料。有文献报道单独应用二磷酸盐后临床症状缓解,而单独应用钙剂和维生素D治疗后病变静止,但两者病灶均无骨化。因此,本病例采取的药物治疗方案可能是治疗MO较理想的选择,尤其是对于无需功能重建手术的患者。大量的临床研究以明确药物的有效治疗剂量及疗程将是必要的,而开展关于MO的多中心临床研究将有助于进一步完善治疗策略。