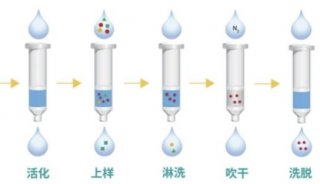
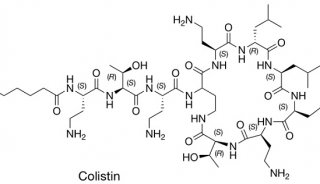
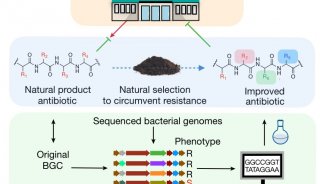
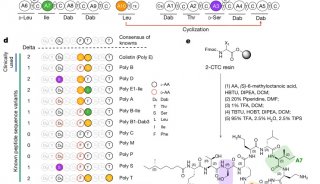
固相合成法制备抗原肽环肽
1.1 仪器与试剂
多肽合成仪(CS536,美国CSBio公司),半制备型高效液相色谱仪(Waters Delta
Prep4000,美国Waters公司),分析型高效液相色谱仪(Agilent 1100,美国Agilent公司),冷冻干燥机(Christ
Alpha,德国Christ公司),激光解吸电离飞行时间质谱仪(LCQ
Deca,美国ThermoFinnigan公司),紫外分光光度计(Beckman
DU7400,美国Beckman公司),C18反相分析柱(Sepax GPC18,5μm,120,4.6mm×150mm)。
实验所用FmocProMerrifield
Resin(取代值0.291mmol/g,交联度1%,100~200目)、BocValWang
Resin(取代值0.523mmol/g,交联度1%,100~200目)、FmocProCTC
Resin(取代值0.42mmol/g,交联度1%,100~200目)、BocTyr(tBu)OH、BocProOH、BocIleOH、BocLeuOH、FmocTyr(tBu)OH、FmocProOH、FmocIleOH、FmocLeuOH、Bocstatine(3s,4s)OH、HATU[O(7偶氮苯并三氮唑1氧)N,N,N′,N′四甲基脲六氟磷酸酯]、HBTU(苯并三唑1四甲基六氟磷酸酯)、HOBt(N羟基苯并三唑)、BOP(邻苯二甲酰丁辛酯)、DIEA(N,N二异丙基乙胺;二异丙基乙胺)、TFA(三氟乙酸)、DMF(二甲基甲酰胺)、DMSO(二甲亚砜)、DCM(二氯甲烷)、ACN(乙腈)、EDC[1乙基3(3二甲氨丙基)碳二亚胺盐酸盐]、NMM(N甲基吗啉)和苯甲硫醚均由杭州中肽生化有限公司提供,哌啶经重蒸后使用,水为二次去离子水。
1.2 HS1及其类似物的化学合成
本文所合成的5种环肽序列分别为:
HS1:cyclo(Ile1Ile2Pro3Pro4Tyr5Val6Pro7
Leu8);
A1HS1:cyclo(Ile1Ile2statine3Pro4Tyr5Val6
Pro7Leu8);
A2HS1:cyclo(Ile1Ile2Pro3statine4Tyr5Val6
Pro7Leu8);
A3HS1:cyclo(Ile1Ile2Pro3Pro4Tyr5Val6
statine7Leu8);
A4HS1:cyclo(Ile1Ile2statine3statine4Tyr5
Val6Pro7Leu8)。
虽然这5种抗原肽环肽或环肽类似物的序列如上面所表示的非常相似,并且按照顺序给每个氨基酸残基做了编号,但考虑到每个化合物的疏水性和空间位阻可能并不完全相同,加之合成的线性肽链终究要环化成抗原肽环肽,因此,为了方便、有效地合成目的产物,我们选择接肽反应的第一个氨基酸也不尽相同。
(1)HS1的合成路线与纯化
树脂溶胀 调用自编程序Method1,树脂溶胀的具体方法是将FmocProCTC Resin 4.76g(合成规模为2.0mmol)用200ml DMF浸泡30min,使之充分溶胀,然后抽干。
脱除氨基保护基 调用自编程序Method2,具体方法为加入含20%哌啶的DMF溶液20ml,搅拌反应30min,再抽干。然后用DMF洗涤5次,以除去残留的脱保护试剂。手工取样,茚三酮检测,若树脂呈深蓝色,则表明Fmoc保护基已经脱除。
接肽反应 调用自编程序Method3,具体方法是在反应器中加入溶解有3.33g FmocValOH的200ml
DMF溶液,机械搅拌2min,然后加入HBTU 3.57g,最后加入NMM
2.02g[AA∶HBTU∶NMM(mol/mol)=3∶2.85∶6],反应30min。抽干,用DMF洗涤3次,然后用甲醇洗涤树脂,以除去氨基酸溶液和DMF,以便手工进行茚三酮检测,检测结果若树脂呈现无色,则说明反应比较完全。依次调用程序Method2和Method3,按肽链的氨基酸序列依次用FmocTyr(2BrZ)OH、FmocProOH、FmocProOH等重复以上接肽反应,直至最终合成出所需肽链。合成顺序为:Pro,Val,Tyr,Pro,Pro,Ile,Ile,L序为:Pro,Val,Tyr,Pro,Pro,Ile,Ileeu。
后续类似物的合成中,表1所列参数基本不变。BocstatineOH的投料比为2,接肽反应时间为40min,脱保护基时间为30min。
肽链的切割
将合成肽链用切割液[TFA∶TIS(triisopropylsilane)∶H2O=95.0∶2.5∶2.5]在低于20℃的条件下切割,反应时间为2.5h,然后减压过滤,收集滤液,用冷乙醚沉淀溶解在切割液中的多肽,4000表1
HS1合成中各氨基酸投料比、接肽反应时间r/min离心3min,真空干燥12h,得线性肽链的粗品约1.5g。
抗原肽肽链的环化
将线性多肽粗品1.4g用200ml
DMF溶解,依次加入EDC(2eq,0.6g)、BOP(1eq,0.7g)、HOBt(2eq,0.42g)和DIEA(5eq,1.1g),过夜环化。加入EDC可以加速缩合反应。蒸干DMF,得环肽粗品1.35g,粗品用MALDITOF质谱仪进行分析鉴定。
环肽粗品的纯化
将上述环化粗品肽溶于适量DMSO中(由于此肽的水溶性不好,上样浓度要严格控制在小于1mg/ml),上样样品用5μm的滤纸过滤。制备色谱柱为Waters
XBridge C18、5μm反相柱;洗脱液:A液为0.1% TFA的水溶液,B液为含0.1%
TFA的乙腈水溶液;检测波长220nm。采用60min内B液由30%~65%的线性梯度洗脱方式,流速为38ml/min。收集纯度高于95%的馏分。最后冷冻干燥,得100mg纯度大于90%的最终产品。
分析型HPLC检测纯度 色谱柱为SepaxGPC18反相柱(4.6mm×150mm,5μm,120);洗脱液:A液为0.1%
TFA的水溶液,B液为含0.1%
TFA的乙腈水溶液;检测波长220nm。采用20min内B液由60%~80%的线性梯度洗脱方式,流速为1.0ml/min。
MS鉴定 激光解吸电离飞行时间质谱仪检测目标产物的分子量。
(2)A1HS1的合成路线与纯化
与HS1的合成略有不同,在A1HS1的合成中,合成方法主要有以下几点变化:①树脂改为FmocProMerrifield
Resin;②氨基酸为Boc保护;③每连接一个氨基酸残基,要用50%
TFA/DCM将肽链切割下来,然后脱保护、洗涤、活化树脂,再连下一个氨基酸残基,最后从树脂上将肽链切割下来的切割液为HF,时间1.2h;④纯化时梯度洗脱条件为B液:70%~100%;⑤HPLC分析时B液:61%~81%;⑥合成顺序为:Pro,Val,Tyr,Pro,statine,Ile,Ile,Leu。其余同HS1合成。冷冻干燥后得250mg纯度大于93%的最终产品。由于溶解度比HS1好,故收率较高。
(3)A2HS1的合成路线与纯化 类似于A1HS1的合成,同HS1的合成相比较,在A2HS1合成中:①树脂为FmocProCTC
Resin;②氨基酸为Fmoc保护;③最后切割液为F液,时间2.5h;④纯化时梯度洗脱条件为B液:65%~90%;⑤HPLC分析时B液:60%~80%;⑥合成顺序为:Pro,Ile,Ile,Leu,Pro,Val,Tyr,statine;⑦因statine是用Boc保护,因此在连接statine后,要将肽链片段先从树脂上切割下来,然后脱保护、洗涤、树脂活化,再连下一个残基。其余同HS1合成。冷冻干燥后得268mg纯度大于92%的最终产品。由于溶解度比HS1好,故收率较高。
(4)A3HS1的合成路线与纯化 类似于A1HS1的合成,同HS1的合成相比较,在A3HS1合成中:①树脂为FmocValWang
Resin;②氨基酸为Fmoc保护;③切割液为F液,时间2.5h;④纯化时梯度洗脱条件为B液:43%~85%;⑤HPLC分析时B液:50%~70%;⑥合成顺序为:Val,Tyr,Pro,Pro,Ile,Ile,Leu,statine;⑦因statine是用Boc保护,因此在连接statine后,要将肽链片段先从树脂上切割下来,然后脱保护、洗涤、树脂活化,再连下一个残基。其余同HS1合成。冷冻干燥后得245mg纯度大于98%的最终产品。由于溶解度比HS1好,故收率较高。
(5)A4HS1的合成路线与纯化 类似于A1HS1的合成,同HS1的合成相比较,在A4HS1合成中:①树脂为FmocProMerrifield Resin;②氨基酸为Boc保护;③每连接一个氨基酸残基,要用50% TFA/DCM切割,然后洗涤,再连下一个氨基酸残基,最后从树脂上将肽链切割下来,切割液为HF,时间1.2h;④纯化时梯度洗脱条件为B液:62%~80%;⑤HPLC分析时B液:62%~82%;⑥合成顺序为:Pro,Val,Tyr,statine,statine,Ile,Ile,Leu;⑦因statine是用Boc保护,因此在连接statine后,要将肽链片段先从树脂上切割下来,然后脱保护、洗涤、树脂活化,再连下一个残基。其余同HS1合成。冷冻干燥后得215mg纯度大于90%的最终产品。由于溶解度比HS1好,故收率较高。
-
科技前沿

-
技术原理

-
会议会展

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
会议会展

-
科技前沿

-
科技前沿

-
标准

-
技术原理
-
项目成果
-
焦点事件

-
焦点事件

-
项目成果

-
焦点事件

-
焦点事件