Flash 案例分享:通过Biotage Isolera 系统分离大极性碱性化合物
在实验室进行柱层析的时候,由于样品的性质的不同,对于所使用的方法就会有所不同,涉及到各种填料以及所对应的各类流动相。对于一些大极性样品而言,我们需要添加一些修饰剂来防止样品拖尾,此次我们将为您分享一个使用Biotage Isolera系统对大极性碱性化合物进行分离纯化的案例。

Flash纯化已成为小分子分离最有效最快速的技术,越来越多的科学家们正依赖Flash加快研发速度,提高速度,降低成本。在实际使用中,对于碱性化合物的纯化而言,由于硅胶填料本身的酸性性质,其保留会变得非常强烈,目标信号峰会出现拖尾现象。最终影响所收集的馏分纯度,同时馏分的溶剂后处理时间也会大大增加。
解决这一问题的办法之一就是在流动相中加入相应的碱性修饰剂,如三乙胺;有时候一些拖尾问题也可以加入第三方溶剂解决,如二氯甲烷(DCM)或者丙酮(Acetone)。Biotage Isolera 全系列拥有第三方溶剂添加系统,可支持最多三种溶剂进行梯度洗脱,这一功能可以很大程度上解决样品溶解性不好的问题,同时部分大极性样品拖尾问题也可以得到缓解。
此次案例中,所使用的样品为尼古丁和咖啡因的混合物,结构如下图:

图1:尼古丁和咖啡因结构图,对应的pKa值分别为:8.5和10.4(40℃)
此次分离,我们进行了三种不同条件的尝试:
· Case1:不带修饰剂的正相硅胶分离
· Case2:添加三乙胺进行的正相硅胶分离
· Case3:使用SNAP KP-NH氨基柱直接分离
实验谱图:
Case 1:不带修饰剂的正相硅胶分离

不加三乙胺的条件下,由于巨大的吸附作用,样品没能够洗脱出来;所使用流动相为正庚烷和乙酸乙酯。
Case 2:通过Isolera系统添加三乙胺进行的正相硅胶分离

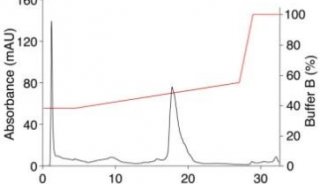
所添加三乙胺的比例为1%,样品成功洗脱出来,不过由于样品极性非常大,整个洗脱过程持续了30 CV(柱体积)。
Case 3:使用SNAP KP-NH氨基柱直接分离

从谱图可以发现,使用了SNAP KP-NH系列氨基柱之后,样品的保留时间大大缩短,新方法只需要13CV即可完成实验,节约了一半以上的溶剂消耗和纯化时间。
结论:
实验发现,在Flash柱层析进行一些大极性化合物纯化时,修饰剂的加入非常必要,同时氨基柱的加入使得此次样品的纯化更加高效快捷,大大节约了溶剂消耗和时间成本;在使用SNAP KP-NH系列色谱柱的时候,不需要再额外添加三乙胺等修饰剂,非常方便。
实验部分:
样品 | 2.0g尼古丁和2.0g咖啡因溶于16mL二氯甲烷溶液当中,得到浓度为0.25g/mL的溶液 |
上样量 | 2 mL (~500 mg) |
色谱柱 | Biotage® SNAP KP-SIL, 25 g |
Biotage® SNAP KP-NH, 28 g | |
系统以及相关设定 | Isolera™ One |
SW 2.1, built: 8789, OS: Biotage 852M | |
254 nm: 收集 | |
280 nm: 检测 | |
信号响应触发值: 100 mAU | |
溶剂 A:正庚烷(Puriss) | |
溶剂 B: 乙酸乙酯(Puriss) | |
Additive: 10 % Triethylamine in n-Heptane | |
平衡 | 3 CV,95% 正庚烷- 5% 乙酸乙酯, 50 mL/min |
梯度 | 1.5 CV 5% 乙酸乙酯 10 CV 5–100% 乙酸乙酯 2 CV 100% 乙酸乙酯 25 mL/min |
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章







