酸碱离解平衡和平衡常数测定
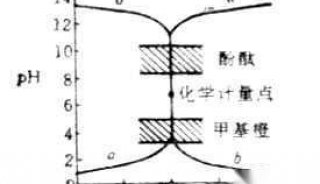
1.只有在醋酸的电离度小于5%时,才能用PH计算醋酸的电离平衡常数。如果电离度大于5%的话,误差会很大。2。不可以这么说。因为此时溶液中的Ac-会水解,HAc会电离,但是c(HAc)一定不等于c(Ac-)。可以跟据c(Na+)+c(H+)=c(Ac-)+c(OH-)电荷守恒,2c(Na+)=c(Ac-)+c(HAc)物料守恒,大致确定c(Ac-)和c(HAc)的关系。3。不等于7。跟Na2CO3溶液呈碱性的原理差不多,醋酸会水解.c- HO2 ====HAc + OH-.4.这两个时候的PH密切反映了醋酸的变化。5。改变温度电离常数一定会变化。因为每个化学反应都伴随着能量的变化。醋酸电离吸热,那么改变温度具体变化如下:T升高,醋酸电离度增大,K增大;T减小,醋酸电离度减小,K减小。可根据 c(H+)c(Ac-) K=----------------- c(HAc) 做出判断:若T增大,则c(H+)c(Ac-)增大,而c(HAc)减小,所以K减小:若T减小,则反之。
推荐
-
焦点事件

-
技术原理
-
技术原理
-
焦点事件

-
焦点事件

-
焦点事件














