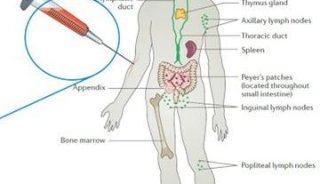
代谢在新一代免疫细胞产品构建中的关键作用

背景介绍BACKGROUND
细胞治疗技术是被认为最有希望攻克肿瘤的创新疗法之一,以CAR-T技术为代表的肿瘤免疫治疗2013年被《Science》杂志评为全球十大科技突破之首。免疫治疗也称为过继细胞治疗(ACT),是基于免疫学原理与方法,采集人体免疫细胞,进行体外培养和扩增,以增强靶向性杀伤功能,再输回人体内,通过调动机体免疫系统杀伤血液与组织中的病原体、癌细胞及突变细胞,抑制肿瘤生长,增强机体免疫能力;细胞免疫治疗是一个复杂的过程,包括细胞提取、细胞分离、细胞培养、质量管控、细胞回输及疗效评估六大环节,每个环节对技术与实验环境均有较高要求。
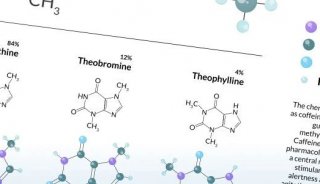
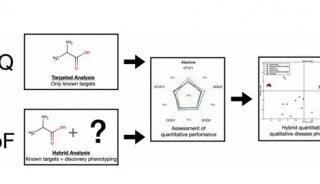
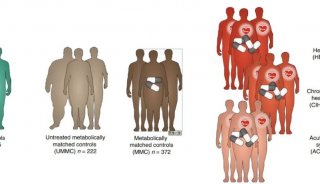
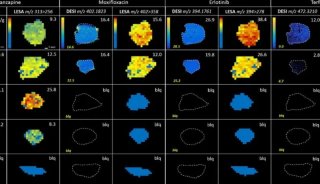
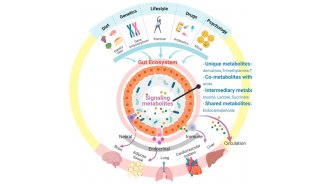
代谢与CAR-T疗法开发稳定、安全和明确表征的细胞生产方法是所有有效细胞疗法的核心,对工程化免疫细胞而言更是如此。在整个生产过程中,必须采用分析方法来引导优化质量属性的关键策略。在治疗细胞生产的不同阶段进行细胞代谢组的测量,包括评估起始材料、转导和活化的细胞以及最终的细胞疗法产品,可以提供有关免疫细胞代谢平衡、表型和效力的深入定性和定量信息。这些数据有助于辅助免疫细胞产品厂家做出明智决策,从而优化生产条件、工艺以及患者所用的细胞治疗产品的质量。实质上来说,代谢调节已成为一项关键工艺指标,用于确定细胞产品是否获得适当质量属性,是否可生产制剂并上市(图1)。

图1. 代谢在新一代免疫细胞产品构建中的关键作用
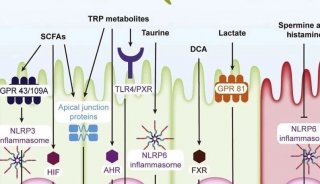
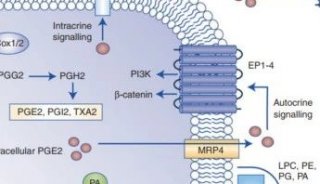
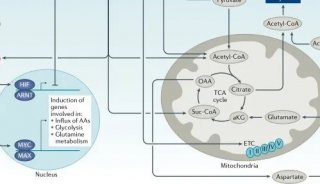
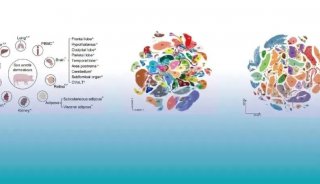
我们总结了与CAR T细胞治疗相关的代谢通路(图2)。

图2:免疫细胞代谢核心通路
糖代谢-多种免疫效应功能
免疫活化是糖酵解通量增加的耗能过程,此过程中机体利用葡萄糖转运体摄取葡萄糖(如GLUT1)后转化为丙酮酸,将NAD+还原为NADH并生成ATP。糖酵解酶如己糖激酶1和2 (HK1和HK2)、甘油醛-3-磷酸脱氢酶(GAPDH)、烯醇化酶和丙酮酸激酶同工酶M2 (PKM2)均可抑制细胞免疫功能。在无氧状态下,细胞通过乳酸脱氢酶(LDH)将丙酮酸还原为乳酸以维持糖酵解通量。Seahorse 分析中,质子和糖酵解衍生的乳酸可通过单羧酸转运体MCT1从细胞中输出时,这种发酵反应称为ECAR。糖酵解在炎症免疫效应细胞中最为活跃,对多种免疫细胞的活化模式至关重要且糖酵解率在B淋巴细胞和T淋巴细胞之间表现不同。
磷酸戊糖途径-在炎性髓细胞中尤为重要
磷酸戊糖途径(PPP)是机体利用葡萄糖直接氧化脱氢脱羧生成NADPH及中间产物为其他物质合成提供原料的过程,G6P脱氢酶为该途径限速酶,生成的NADPH在免疫细胞中有多种生物学效应。中性粒细胞和炎症巨噬细胞可利用PPP及NADPH产生活性氧(ROS)发挥抗感染作用。NADPH还可作为抗氧化剂防止组织细胞的过度损伤。
TCA循环和ETC为代谢的核心枢纽
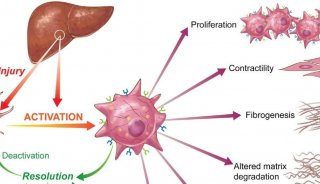
TCA循环和线粒体电子传递链(ETC)生成的能量对机体代谢至关重要。与糖酵解相比,OXPHOS生成能量更有效且与体内免疫细胞的寿命有关。在巨噬细胞促炎活化过程中,TCA循环通过下调IDH和SDH活性而被重构,后者通过活化髓细胞中ACOD1/IRG1产生特异性免疫调节代谢物衣康酸直接抑制而实现。
脂肪酸代谢-支持免疫细胞的表型和功能
脂肪酸氧化(FAO)是肉碱棕榈酰转移酶1和2 (CPT1和CPT2)将长链脂肪酸转运到线粒体基质后经羟酰基辅酶a氧化为乙酰辅酶a、NADH和FADH2并生成能量的过程。高浓度的CPT1抑制剂依托莫西实验表明FAO在IL-4诱导的巨噬细胞、记忆性T细胞和调节性T细胞(Tregs)中尤为重要。然而,最近对CPT1和CPT2应用细胞特异性基因敲除的文献报道表明,FAO在此过程中很少。
与FAO相反,FAS是乙酰辅酶a羧化酶(ACC)将乙酰辅酶a羧化为丙二酰辅酶a,后脂肪酸合酶(FASN)将丙二酰辅酶a延长为脂质的合成过程。FAS支持效应T细胞增殖,是配置巨噬细胞炎症信号的质膜的关键,也是促进活化的DCs分泌细胞因子的关键。
氨基酸代谢-在不同免疫细胞间代谢存在差异
T细胞免疫活化与氨基酸代谢需求增加相关;氨基酸在调节免疫反应的特定方向也发挥一定作用, 氨基酸在炎性巨噬细胞中也有重要的调节功能,此外,氨基酸可促使巨噬细胞产生效应分子。
谷氨酰胺
活化的T细胞和巨噬细胞可上调谷氨酰胺代谢,以维持细胞存活和免疫反应。如Th1和Th17细胞通过转运蛋白ASCT2可增加谷氨酰胺用量应对抗原刺激,抗炎Treg则不受谷氨酰胺供应改变的影响。谷氨酰胺酶(GLS)将谷氨酰胺转化为谷氨酸为TCA循环提供燃料,该途径可促进Th17分化,同时降低Th1和细胞毒性T淋巴细胞的分化程度。
精氨酸
精氨酸代谢在T细胞活化和免疫反应调节中也有重要作用,在炎症反应消除过程中,免疫调节细胞通过精氨酸酶1 (ARG1)的表达促进精氨酸降解。
色氨酸
炎症还可以通过吲哚胺2,3-双加氧酶(IDO)和色氨酸2,3-双加氧酶(TDO) 等酶介导的色氨酸代谢得到解决。巨噬细胞IDO表达也通过产生犬尿氨酸为NAD+的合成提供原料,从而维持其抗炎和吞噬功能。值得注意的是,在巨噬细胞中,犬尿氨酸的产生可以维持线粒体适应度和OXPHOS。此外,IDO抑制可能不仅在免疫抑制和/或肿瘤前TAMs中损害NAD+的生成,而且在CD8+TILs中也可能损害NAD+的生成。重要的是,NAD+的产生是维持T细胞免疫反应的一个关键代谢物。
脂肪酸和胆固醇代谢-关键能量来源
免疫细胞通常会提高从头合成脂肪酸的速度为细胞膜上的磷脂和信号分子的生成提供能量,有效的免疫突触的形成对T细胞功能至关重要,而这依赖于细胞膜的脂质组成。此外,不同脂肪酸对CD4+T细胞的分化和增殖有不同影响,如长链脂肪酸月桂酸可维持促炎Th1细胞和Th17细胞分化,短链脂肪酸丙酸则促进Treg细胞发育。因此,TME中存在的脂质种类可能改变效应细胞CD4+T细胞的浸润模式,并可能决定靶向脂质代谢治疗肿瘤的效果。M1型和M2型巨噬细胞之间的脂质代谢也不同,比如脂肪酸合成主要发生在M1型巨噬细胞中,而M2型巨噬细胞依赖于脂肪酸氧化(FAO)来满足其生物能量需求。
下期看点
氨探生物开发的一站式细胞非靶向代谢组学平台为生物制药行业提供了一种高效的免疫细胞产品质量控制解决方案。通过严格验证的超高灵敏度质谱检测平台和精准、深度的代谢物数据库比对,提高了细胞非靶向代谢组学检测的可靠性,期待我们的方案为生物制药企业提升产品开发的效率。
1.Liang L, Sun F, Wang H, Hu Z. Metabolomics, metabolic flux analysis and cancer pharmacology. Pharmacol Ther. 2021 Aug;224:107827.
2.Xiaoyun Li et al. Navigating metabolic pathways to enhance antitumour immunity and immunotherapy. Nature Reviews Clinical Oncology (2019).
3.Leone RD, Powell JD. Fueling the Revolution: Targeting Metabolism to Enhance Immunotherapy. Cancer Immunol Res. 2021 Mar;9(3):255-260. doi: 10.1158/2326-6066.CIR-20-0791. PMID: 33648947; PMCID: PMC8240594.
Untangled Biosciences解构健康奥秘、探寻生命答案,氨探生物以一流的分子表型组平台和成熟的临床转化应用体系,为优秀的研究团队进行技术和数据赋能,致力于实现分子表型水平的精准诊疗。

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章