辉瑞第5款阿达木单抗生物仿制获美国FDA批准!
辉瑞(Pfizer)研制的一款生物类似药Abrilada (adalimumab-afzb,阿达木单抗)近日获得美国FDA批准,该药是艾伯维旗舰产品修美乐(Humira,通用名:adalimumab,阿达木单抗)的生物仿制药,用于治疗多种自身免疫性疾病,包括:类风湿性关节炎(RA)、幼年特发性关节炎(JIA)、银屑病关节炎(PsA)、强直性脊柱炎(AS)、成人克罗恩病(CD)、溃疡性结肠炎(UC)、斑块型银屑病。

此次FDA批准,基于对一个综合数据包的审查,该数据包证明了Abrilada相对于参考药物Humira的生物相似性。其中包括REFLECTIONS B538-02临床对比研究的结果。这是一项随机、双盲、平行组III期临床研究,在接受甲氨蝶呤(MTX)治疗缓解不足的中度至重度活动性类风湿性关节炎(RA)患者中开展,评估了Abrilada皮下注射用药(每隔一周皮下注射40mg)联合甲氨蝶呤治疗方案相对于Humira皮下注射用药(每隔一周皮下注射40mg)联合甲氨蝶呤治疗方案的疗效、安全性及免疫原性。结果显示,Abrilada与Humira在疗效、安全性、免疫原性方面没有发现有临床意义的差异。
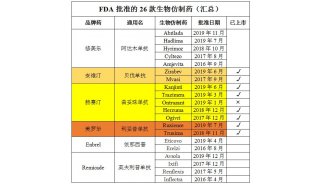
截至目前,FDA共批准了25个生物仿制药。Abrilada是FDA在2019年批准的第9个生物仿制药,也是该机构迄今为止批准的第5个阿达木单抗生物仿制药。
除了辉瑞Abrilada之外,其他4款已批准的阿达木单抗生物仿制药分别为:Hadlima(三星Bioepis/默沙东,2019年7月)、Hyrimoz(诺华山德士,2018年10月)、Cyltezo(勃林格殷格翰,2017年8月)、Amjevita(安进,2016年9月)。
-
企业风采

-
投融资

-
市场商机

-
焦点事件

-
焦点事件

-
焦点事件

-
市场商机

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
会议会展

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
财报

-
焦点事件

-
企业风采

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
会议会展

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
科技前沿

-
焦点事件

-
焦点事件

-
政策法规

-
焦点事件

-
科技前沿
-
焦点事件

-
焦点事件

-
科技前沿

-
焦点事件

-
科技前沿
-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件
-
科技前沿
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
市场商机
-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采
-
科技前沿
-
科技前沿

-
科技前沿

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
焦点事件

-
科技前沿

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
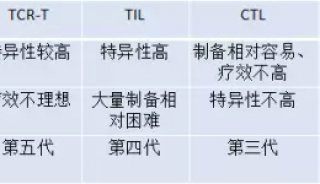
技术原理
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果
-
项目成果

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果

-
焦点事件
-
项目成果

-
焦点事件
-
焦点事件

-
焦点事件
-
焦点事件
-
焦点事件

-
焦点事件
-
产品技术
-
企业风采

-
焦点事件

-
并购

-
市场商机

-
市场商机

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
焦点事件

-
产品技术

-
企业风采

-
焦点事件

-
焦点事件