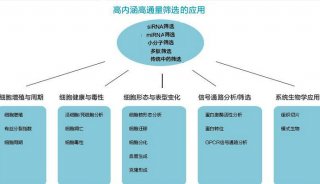
魏文胜:CRISPR功能性筛选新方法
自2013年Science杂志将CRISPR技术选为年度突破开始,这一新技术就给基因编辑世界带来一场风暴:在过去的这一年半时间里,CRISPR方法已迅速席卷了整个动物王国,成为DNA突变和编辑的一种明星技术。
国内外各大生物实验室的科学家们纷纷尝试利用这种技术进行攻关,近期来自北京大学生命科学学院的研究人员就取得了一项阶段性的重要成果,开发了一种基于 CRISPR/Cas9系统的慢病毒聚焦型人源细胞文库、功能性基因筛选平台以及基于高通量深度测序技术解析数据的完整技术路线。
那么这一套技术路线是什么?相对于其它方法有哪些优势?这项研究对于基础研究和临床研究又具有哪些意义呢?为此生物通特联系了领导这一研究的魏文胜研究员,就读者感兴趣的问题请教了他。
明星技术CRISPR/Cas9系统
近年来基因组编辑领域取得飞速的发展,锌指核酸酶(ZFNs)、转录激活因子样效应物核酸酶(TALENs)、CRISPR/Cas系统大大改变了科研人员在哺乳动物系统中研究基因及其功能的方式。
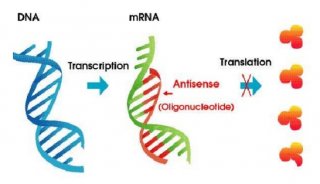
CRISPR/Cas系统最初被发现是细菌和古细菌为抵御病毒和质粒不断攻击而演化来的一种获得性免疫防御机制。在II型CRISPR/Cas系统中,Cas9内切酶家族在单导向RNA (single-guide RNA,sgRNA)引导下靶向和剪切外源基因,生成DNA双链断裂(DSBs)。CRISPR/Cas系统系统的高效基因组编辑功能已被应用于多种生物,包括人、小鼠、大鼠、斑马鱼、秀丽隐杆线虫、植物及细菌。相比于ZFNs和TALEN, CRISPR/Cas系统介导的基因组靶向实验在真核细胞中具有相似甚至更高的效率。
在这项最新研究中,魏文胜研究员就是采用了这一系统,开发了一种慢病毒聚焦型人源细胞文库、功能性基因筛选平台,并由此结合高通量深度测序技术,获得了一种高效的新型遗传筛选技术。
魏文胜研究员表示,“CRISPR/Cas9技术是造成基因完全敲除来产生表型差异,而RNA干扰是基因表达的下调,概念上完全不同。所以前者可以很好的解决后者的问题。 而TALENs不适合,因为TALENs work in pairs, 而且不能通过慢病毒侵染方式建库(会发生重组突变)”。
新型遗传筛选技术鉴定宿主受体
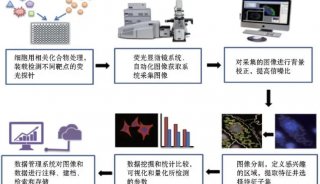
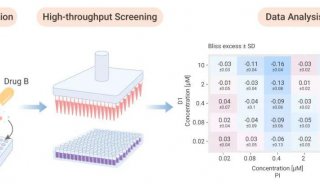
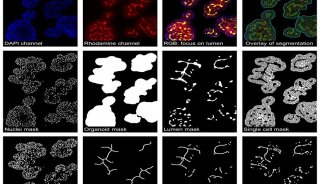
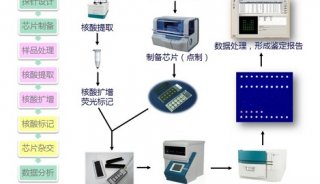
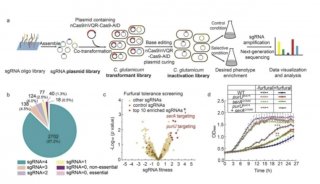
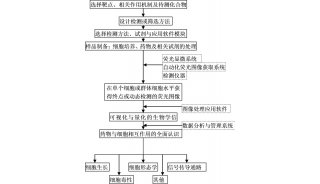
构建这一套高效的遗传筛选技术,“简单的讲,包括预先建立稳定表达Cas9(以及OCT1)的细胞系并确定sgRNA能够在该细胞系实现基因修饰;建立sgRNA慢病毒文库以及细胞文库;功能性筛选和富集;PCR扩增和深度测序分析;数据分析及候选基因的验证 等等”,魏文胜研究员解释道。
通过这一套技术,魏文胜研究员和他的同事成功地鉴别出了对于炭疽和白喉毒素毒性至关重要的宿主基因,并在随后的细胞实验中对这些候选基因进行了进一步的功能验证。
研究发现了与病菌侵染宿主蛋白及通路有关的基因,这将为对抗病菌提供了新型药物靶点 ,而且更重要的是,这一强大的高通量基因筛选技术的建立可以用于广泛的生物学问题研究,惠及众多生物医学相关研究领域。
具体来说,这种基于CRISPR的策略结合深度测序分析适用于功能基因组学研究,广泛地利用这一强有力的遗传筛选策略,将能进一步地推动以一种高通量的方式应用CRISPR/Cas系统开展基因功能研究,不仅能够快速地鉴别对细菌毒性至关重要的基因,还将促成发现参与其它生物过程的基因。
同时,这项具有里程碑意义的工作与已经在Science杂志发表的两篇主题相近的文章比较,该工作所报道的方法具有更为广泛的细胞系适应性,对于功能性基因的筛选和鉴定具有十分重要的意义。
-
企业风采

-
科技前沿

-
焦点事件

-
项目成果

-
综述
-
项目成果
-
焦点事件
-
产品技术
-
产品技术
-
综述
-
科技前沿

-
综述

-
综述
-
焦点事件

-
企业风采

-
科技前沿

-
焦点事件

-
项目成果

-
科技前沿

-
焦点事件

-
焦点事件
-
项目成果

-
项目成果
-
技术原理
-
技术原理

-
焦点事件

-
焦点事件

-
项目成果
-
综述

-
焦点事件
-
综述
-
投融资

-
焦点事件

-
技术原理