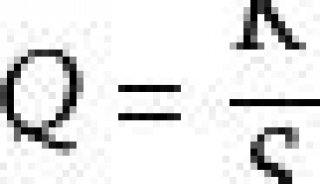底物浓度对催化反应速度的影响及米氏常数Km 和最大 ...
底物浓度对催化反应速度的影响及米氏常数Km 和最大 反应速度Vmax的测定实验
实验方法原理
根据Michaelis-Menten 方程:
可以得到Lineweaver-Burk 双倒数值线方程:
在 1/ V 纵轴上的截距是1/ Vma x , 在1/ [ S ] 横轴上的截距是- 1/ Km 。
测定Km 和Vmax , 特别是测定Km , 是酶学研究的基本内容之一, Km 是酶的一个基本的特性常数, 它包含着酶与底物结合和解离的性质, 特别是同一种酶能够作用于几种不同的底物时,米氏常数Km 往往可以反映出酶与各种底物的亲和力强弱, Km值越大, 说明酶与底物的亲和力越弱, 反之, Km 值越小, 酶与底物的亲和力越强。
双倒数作图法应用最广泛, 其优点是: ① 可以精确地测定Km 和Vma x ; ② 根据是否偏离线性很容易看出反应是否违反Michaelis-Menten 动力学; ③ 可以较容易地分析各种抑制剂的影响。此作法的缺点是实验点不均匀, V 小时误差很大。
建议采用一种新的Eisenthal 直线作图法, 即将Michaelis-Menten 方程改变为:
作 图时, 在纵轴和横轴上截取每对实验值: V1 ~ [ S ] 1 ;V2 ~ [ S ]2 ; V3 ~ [ S] 3 ; ———连接诸二截点, 得多条直线相交于一点, 由此点即可得Km 和Vmax 。
此作图法的优点是: ① 不用作双倒数计算; ② 很容易识别出那些不正确的测定结果。
还可以用Hanes 方程进行作图, 斜率是1/ Vma x , 截距分别是- Km 和Km/ Vma x :
实验材料 蔗糖
试剂、试剂盒 乙酸缓冲液葡萄糖果糖蔗糖二硝基水杨酸溶液
仪器、耗材 分光光度计水浴锅试管保鲜膜
实验步骤
1. 本实验和下一个实验均采用二硝基水杨酸法测量反应产物还原糖, 为了掌握该法测定的范围, 可先作一条标准曲线。按下面的“ 表1” 进行实验操作:
用第1 管作空白对照, 测定其余各管520 nm 的吸光度A520 。用A520 值对还原糖的μmole 数作图。
2. 按下面的“表2”测定不同底物浓度对催化速度的影响。
为使Km 测准, 必须先加蔗糖, 精确移液, 准确计时, 每隔30 秒钟或1 分钟加酶一次, 加酶后要摇动一下试管,每支试管
都要保证准确反应5 min , 然后加1.0 ml 二硝基水杨酸试剂, 立即用保鲜膜盖住管口, 绕上橡皮筋, 用针刺一小孔, 几根试管用一根橡皮筋套住放入沸水浴, 煮5 min 后取出放入冷水中速冷。最后加3.0 ml H2O, 充分摇匀, 必要时可用一小块保鲜膜盖住管口, 反复倒转试管, 混匀。用比色杯测定时, 空白对照管溶液必须充分摇匀, 彻底除去气泡, 测A520 值时要检查参比杯内壁上是否有气泡, 若有, 须倒回原试管, 再摇动除去残余气泡。实验中不允许用嘴吸试剂。实验完毕后要注意洗手。
3. 第9、10 二管先加中止反应的NaOH 溶液, 后加酶, 以保证加酶后不再产生任何还原糖, 用以校正蔗糖试剂本身的水解和酸水解。用第9、第10 二管的数据画一直线, 求出其他各管的校正数据, 对所测各管的A520 值进行校正, 然后计算每管的[ S ] , 1/ [ S] , V 和1/ V。
4. 画出反应速度V 与底物浓度[ S ] 的关系图(米氏曲线)和1/ V-1/ [ S ] 双倒数关系图(不要直接用A520 值作图) , 计算
Km 和Vmax , 并与文献值进行比较。实验结果记录时, 要将[ S ] 和V 的单位表示清楚, 并列出反应速度的计算公式。
-
焦点事件

-
科技前沿

-
焦点事件
-
科技前沿
-
科技前沿
-
技术原理
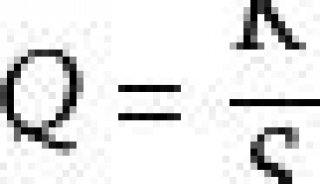
-
焦点事件
-
焦点事件

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件