今年第一笔,阿斯利康持续扫货中国创新药
1月2日,安锐生物(Allorion Therapeutics)宣布与阿斯利康达成独家选择权和全球许可协议,开发并商业化一款针对表皮生长因子受体(EGFR)L858R突变的新型变构抑制剂,用于治疗晚期EGFR突变的非小细胞肺癌(NSCLC)。
根据协议条款,阿斯利康将获得一款新型EGFR L858R变构抑制剂的全球开发和商业化的独家授权。安锐生物将有权获得高达4000万美元的预付款和近期付款,超过5亿美元的研发和商业化里程碑付款,以及全球净销售额的分级特许权使用费。
此次交易是阿斯利康今年第一次引进国产新药。作为深耕中国市场的MNC,阿斯利康近年来开始频繁扫货国产潜力创新药,据动脉橙果局的不完全统计,2023年阿斯利康与国内企业达成了6项合作交易,在ADC管线、代谢疾病领域以及细胞治疗领域进行了多点布局。
安锐生物成立于2020年,是一家专注于癌症和自身免疫性疾病新型小分子药物研发的生物技术公司,在美国波士顿和中国广州均建有研发中心。公司拥有一支经验丰富的药物发现和开发团队,创始团队由多位平均具有15年工作经验的国际顶尖药企或Biotech研发与管理经验的科学家和创业者组成。
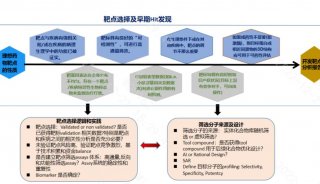
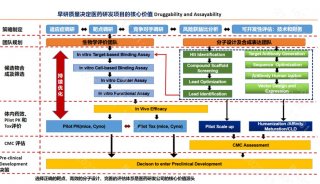
在技术平台方面,安锐生物建立了独特的早期发现平台,包括变构抑制剂筛选平台和基于表型筛选和结合CRISPR技术的合成致死分子发现平台,并且构建了包含近20万个高质量小分子的化合物文库。
此次合作重点的新型EGFR L858R变构抑制剂是安锐生物在肿瘤领域推出的全新管线,旨在解决当前EGFR抑制剂的耐药性问题。根据公司新闻稿,该款EGFR L858R变构抑制剂具有在联合用药时增强其疗效的潜力。而此次与阿斯利康的合作将加速其进入临床,并探索与其他EGFR靶向分子如奥希替尼(Tagrisso)的潜在治疗组合。
除此之外,安锐生物在三年多的时间李布局了多个差异化的小分子创新药研发管线,进展较快的是两款进入Ⅰ/Ⅱ期临床试验阶段的产品——TYK2抑制剂和CDK2抑制剂。其中,TYK2抑制剂目前获批临床的适应症为成人中-重度斑块型银屑病,CDK2抑制剂则用于治疗卵巢癌、子宫内膜癌和乳腺癌等实体瘤。
奥希替尼是阿斯利康研发的第三代口服、不可逆的选择性EGFR突变抑制剂,是全球第一个上市,也是中国首个获批的用于EGFR T790M突变阳性的局部晚期或转移性NSCLC的肿瘤药物,也是目前EGFRm NSCLC一线治疗的标准治疗。
奥希替尼是阿斯利康的王牌药物,并且是目前EGFR小分子药物中最畅销产品,2022年其销售额达到54.4亿美元,同比增长8.5%,居阿斯利康产品销售额榜首,成为全球第六大抗肿瘤药物。2023年前三季度奥希替尼销售额达43.8亿美元,全年有望突破60亿美元。
不过,畅销的奥希替尼也成了“众矢之的”。而奥希替尼治疗后出现的耐药性问题仍未有解决办法,目前也尚未有在奥希替尼耐药后的靶向治疗获批上市。因此,各大药企抓住这一点纷纷涌入EGFR药物市场,并陆续开展了与奥希替尼的头对头试验。
强生便是其中一个强劲对手。
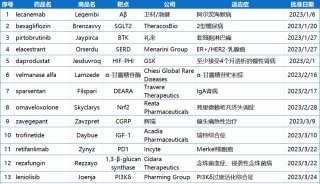
强生研发的EGFR MET双抗埃万妥单抗(Rybrevant)于2021年5月被美国FDA批准上市,用于治疗铂类化疗后进展的EGFR外显子20插入突变的转移性NSCLC患者。2021年,强生与韩国生物制药企业Yuhan Pharmaceutical达成合作,引进了第三代EGFR抑制剂拉泽替尼(LECLAZA)。
在2023 ESMO大会上,强生公布了一项针对奥希替尼的头对头Ⅲ期临床试验,数据显示,埃万妥单抗和拉泽替尼联用能比奥希替尼疾病进展或死亡的风险降低30%;中位无进展生存期(PFS)达到23.7个月,比奥希替尼多7.1个月;总生存期(OS)数据尚未成熟,但表现出了积极趋势。
此外,在NSCLC中,HER3表达与晚期疾病、转移时间缩短和生存率降低有关,并且HER3的高表达也与EGFR TKI耐药相关。基于此,第一三共研发了全球首款靶向HER3的新一代ADC药物——Patritumab deruxtecan(HER3-DXd,U3-1402),以期解决奥希替尼耐药性问题。
HER3-DXd的Ⅰ期临床试验研究结果显示,在经过重度预治疗的患者群体中,客观缓解率达39%,中位缓解持续时间为6.9个月,中位PFS为8.2个月。其在对EGFR TKI耐药的EGFRm NSCLC患者中表现出持久的抗肿瘤活性。
2021年,第一三共开展了一项全球性、多中心、开放标签的Ⅱ期试验,评估HER3-DXd在具有EGFR激活突变的转移性或局部晚期NSCLC患者中的有效性和安全性,这些患者的疾病在奥希替尼、第三代EGFR TKI和≥1铂类化疗方案或之后耐药。
其试验结果显示,每3周1次的HER3-DXd显示出临床意义上的疗效和持久的颅内缓解,在既往接受过治疗的EGFR突变NSCLC患者中具有可管理的安全性,在以是否存在脑转移、肿瘤HER3表达、EGFR TKI治疗的耐药机制及是否存在脑转移为特征的亚组分析中显示出跨亚组的临床获益。
除此之外,尽管奥希替尼的化合物专利至2032年7月才到期,但国内早已有仿制药获批上市。2023年10月,江苏万邦生化医药集团(“万邦医药”)的4类仿制化药甲磺酸奥希替尼片获批上市,为国内首款获批的奥希替尼仿制药。
不过在原研专利未到期或专利未被挑战成功前,万邦医药的仿制药暂时未能上市销售,奥希替尼目前也并未受到仿制药的威胁。但是目前国内也已有3个Me-too第三代EGFR-TKI获批上市,分别是阿美替尼(豪森药业)、伏美替尼(艾力斯)、贝福替尼(贝达药业)。
面对众多对手的“围堵”,阿斯利康没有坐以待毙,而是通过引进新药、联合用药、拓宽适应症等方式来解奥希替尼的“被围之困”。
2023年9月,奥希替尼片新适应症在国内的上市申请获得受理。同样在9月的2023 世界肺癌大会(WCLC)上,阿斯利康公布了奥希替尼的Ⅲ期临床试验结果。数据显示,相较于奥希替尼一线单药疗法,联用化疗将中位PFS延长了8.8个月、将疾病进展风险降低了38%。虽然目前OS数据暂未成熟,但已表现出有利趋势。
围绕奥希替尼联合用药方案,阿斯利康布局了包括用于辅助治疗的ADAURA、ADAURA2,新辅助治疗的NeoADAURA,一线治疗的FLAURA等多个对耐药问题展开的临床研究。预计在2024年度,Ⅲ期临床试验FLAURA、NeoADAURA研究、Ⅱ期临床试验SAVANNAH的结果将陆续公布。
这一次引进安锐生物的新型EGFR L858R变构抑制剂,与奥希替尼联合用药或将带来更好的疗效。
此外,在新药研发方面,阿斯利康开发了EGFR/c-MET双靶点ADC新药AZD9592,临床前研究结果显示,AZD9592具有可观的疗效和安全性,代表了多种临床环境中的不同机会。
2023年5月,AZD9592的临床试验获得国家药监局药品审评中心(CDE)默示许可,拟用于单药和与抗癌药物联合用药治疗晚期实体瘤。如若顺利推进,AZD9592单药或联用奥希替尼将成为解决奥希替尼耐药问题的重要方案。
-
企业风采

-
投融资
-
企业风采

-
焦点事件
-
实验室动态

-
焦点事件
-
企业风采

-
焦点事件

-
科技前沿
-
企业风采

-
财报

-
焦点事件
-
焦点事件
-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
投融资

-
焦点事件

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
会议会展

-
会议会展
-
焦点事件

-
企业风采

-
会议会展

-
企业风采

-
精英视角

-
焦点事件
-
财报
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿
-
企业风采

-
焦点事件

-
会议会展

-
焦点事件

-
焦点事件

-
精英视角

-
焦点事件

-
企业风采

-
会议会展

-
焦点事件

-
科技前沿

-
焦点事件

-
企业风采

-
焦点事件
-
市场商机
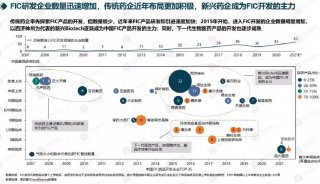
-
市场商机
-
科技前沿

-
科技前沿

-
科技前沿
-
企业风采

-
科技前沿
-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
焦点事件

-
科技前沿

-
焦点事件

-
招标采购

-
焦点事件
-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果
-
精英视角

-
焦点事件

-
焦点事件
-
焦点事件

-
精英视角

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
市场商机
-
焦点事件

-
焦点事件

-
企业风采

-
产品技术

-
企业风采
-
焦点事件
-
项目成果

-
科技前沿

-
科技前沿
-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
并购

-
焦点事件

-
焦点事件

-
综述
-
焦点事件
-
焦点事件

-
焦点事件
-
产品技术

-
产品技术
-
产品技术

-
项目成果
-
产品技术

-
产品技术
-
产品技术
-
市场商机

-
焦点事件

-
焦点事件

-
科技前沿
-
焦点事件