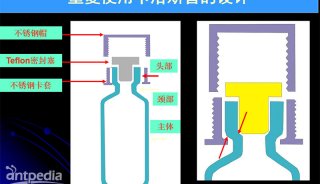
外泌体在肝纤维化过程中发挥的作用研究
过分!外泌体连肝纤维化也掺和!
关于IL-17 (白介素-17) 对肝脏疾病的作用,科学家们已经研究得很透彻了,但尚不知道IL-17的来源,特别是在非病原体引起的肝损伤和纤维化。今天我们来看看,来自韩国KAIST的研究者在Hepatology上叙述的一个关于外泌体与肝纤维化的故事。
受到肝损伤后,肝细胞分泌的外泌体会含有多种self-RNA (自身RNA)。最近,科学家发现self-ncRNA是toll 样受体3 (TLR3) 的催化剂。研究者使用TLR3 KO小鼠和野生型小鼠,注射CCl4 (四氯化碳) 引起肝纤维化,发现TLR3 KO小鼠的IL-17A水平、纤维相关的介质减少,表明这种肝损伤与IL-17A产量、TLR3有关。
肝纤维化, 怎样引起IL-17A生成?
研究者通过对细胞因子染色,发现在急性肝损伤时,肝γδT细胞 (其受体由γ和δ链组成的T细胞) 是IL-17A的主要生产者,且它的细胞数量在肝纤维化TLR3 KO小鼠中显著减少,这可能就是早期肝纤维化IL-17A减少的原因。
γδT细胞中这么多IL-17A, 从何而来?
一般情况下,IL-17A主要由CD4+ T helper产生。这不免让大家好奇γδT细胞是怎样产生IL-17A的。
研究者将表达eGFP的γδT细胞过继转移 (adoptive transfer) 到纤维化的肝脏,发现只有0.1%的肝淋巴细胞能转运γδT细胞,其余大部分与激活的HSC细胞 (肝星状细胞) 密切接触,提示HSC细胞在此过程中发挥作用。于是研究者开始对它的研究:敲除HSC细胞的TLR3后,IL-17A, IL-1β, IL-12p40和IL-23p19减少,表明HSC细胞中的TLR3激活,竟然与肝损伤及纤维化对γδT细胞的募集与激活有关!
HSC与γδT细胞以什么联系?难道是…
没错,研究者想到了外泌体 (exo) 。研究者首先检测了exo是否会影响上述相关基因的表达。

CCl4处理肝癌细胞,12h后提取细胞培养基中的exo (下称CCl4-exo),孵育HSC细胞24h

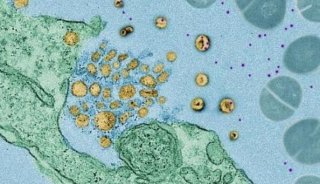
Dil标记exo,观察得许多exo进入了HSC胞内

CCl4-exo提高了这些基因在HSC细胞的表达,这样IL-1β和IL-23就能增加γδT细胞,增加IL-17A产量
研究者还发现,TLR3激活休眠的HSC后,会增加RORγt表达,提高γδT细胞的IL-17A生成量;通过TLR3 KO骨髓移植筛选建立的没有TLR3的嵌合小鼠中,IL-17A+ γδT细胞减少。
表达IL-17需要exo激活HSC的TLR3?

用CCl-4刺激Hep3B和hES-Hep细胞,提取exo (即CCl4-exo) ,与HSC细胞株LX-2或hTert共培养24h,qPCR结果显示CCl4-exo增加了两种细胞的IL-17A表达。

对敲降TLR3或正常的LX-2细胞,进行exo或者poly I:C处理 (能激活TLR3),进行qPCR。exo或poly I:C处理提高了IL-17A表达,而敲降TLR3后IL-17A减少。

本研究阐述了肝纤维化早期阶段,先天γδ T细胞是IL-17A的主要来源,这一点反映在γδ T细胞与HSC细胞的相互作用 (TLR3能介导HSC细胞生成IL-17A)。研究者猜测,肝损伤后产生未知的self-TLR3配体,进入exo,exo以此激活HSC细胞的TLR3,提高γδ T细胞的IL-17A,加剧肝纤维化。
原文:Seo W, et al. Exosome-Mediated Activation of Toll-Like Receptor 3 in Stellate Cells Stimulates Interleukin-17 Production by γδ T cells in Liver Fibrosis. Hepatology. 2016 May 14.
-
科技前沿
-
焦点事件

-
焦点事件

-
项目成果
-
科技前沿
-
焦点事件

-
产品技术

-
科技前沿

-
科技前沿
-
政策法规
-
科技前沿

-
技术原理

-
项目成果
-
项目成果
-
项目成果

-
项目成果
-
焦点事件

-
科技前沿
-
项目成果
-
焦点事件

-
项目成果

-
项目成果

-
项目成果
-
科技前沿
-
项目成果

-
会议会展

-
焦点事件