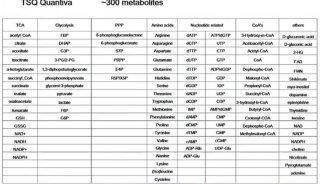
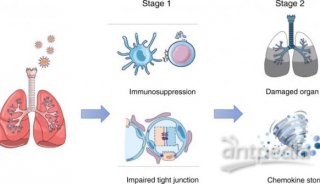
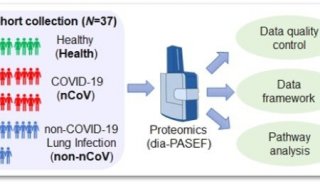
RNAi表达载体构建
近年来的研究表明,一些短片断的双链RNA可以通过促使特定基因的mRNA降解来高效、特异的阻断体内特定基因表达,诱使细胞表现出特定基因缺失的表型, 称为RNA干扰(RNA interference,RNAi)。siRNA(small interfering RNAs)就是这种短片断双链RNA分子,能够以序列同源互补的mRNA为靶目标,降解特定的mRNA。RNAi的发现具有划时代的意义,它不仅深入揭示 了细胞内基因沉默的机制,而且它还是后基因组时代基因功能分析的有力工具,极大地促进了人类揭示生命奥秘的进程。现在越来越多的研究人员开始采用RNAi 来研究生物体的基因表达。RNAi技术可广泛应用到包括功能基因组学,药物靶点筛选,细胞信号传导通路分析,疾病治疗等等。
目前为止较为常用的5种制备siRNAs的方法包括
· 化学合成
· 体外转录
· 长片断dsRNAs经RNase III 类降解 (e.g. Dicer, E. coli, RNase III)
· siRNA表达载体或者病毒载体在细胞中表达siRNAs
· PCR制备的siRNA表达框在细胞中表达
五种方法优缺点比较如下:
比较项目 | 化学合成 | 体外转录 | RNase III降解dsRNA | siRNA | PCR |
材料需求 | 21-mer RNA | 29-mer DNA oligos(一对) | 转录模版 (200-1000bp,两侧带T7 启动子) | 55-60-mer DNA oligos(一对) | ~50-mer DNA oligos(一对) |
全部制备/合成时间所需时间 | 4天—2周 | 24 小时 + DNA oligo合成时间 | 1 天 + 转录模版制备时间 | 5天以上 + DNA oligo合成时间 | ~ 6 小时 + DNA oligo合成时间 |
个人所需操作时间 | 几乎不需要* | 中等 | 中等 | 多 | 中等 |
是否需要验证和寻找最有效siRNA | 需要 | 需要 | 不需要 | 需要 | 需要 |
能否标记siRNA (例如用于荧光显微镜分析siRNA进入细胞过程或者在细胞中的定位) | 能 | 能 | 能 | 不能 | 不能 |
转染的相对难易程度 | 好 | 好 | 好 | 差 | 差 |
可筛选性 (例如抗生素筛选) | 不可以 | 不可以 | 不可以 | 可以 | 不可以 |
能否用于长效抑制 | 不可以 | 不可以 | 不可以 | 可以(抗生素筛选) | 不可以 |
能否大规模制备 | 可以 | 有限 | 有限 | 可以 | 有限 |
检测总体转染效率 | 不可以 | 不可以 | 不可以 | 可以 | 不可以 |
每个基因的相对费用(不包含人力) | 高 | 中等 | 低 | 中等 | 中等 |
*取决于合成后是否包含纯化、去保护,以及厂家提供的是已经退火的即用型双链还是冻干的单链 | |||||
RNAi研究的一般技术路线是:
由上述的路线可以看出,获得高纯度的siRNA产物是进行实验的第一步,而转染的效率则是非常关键的因素。
一、基本概念:
Ø RNAi:(RNA interference)RNA干扰
内源性或外源性双链RNA(dsRNA)介导的能诱导细胞内与其序列同源的特异基因表达沉默或抑制的效应,诱使细胞表现出特定基因缺失的表型,称为RNA干扰,它也是体内抵御外在感染的一种重要保护机制。
Ø siRNA :(small interfering RNAs)小干扰RNA
由长dsRNA裂解而成的一种19-25nt的短片断双链RNA分子,能够以同源互补序列的RNA为靶目标降解特定的mRNA, RNAi的关键效应分子。
Ø shRNAs:(small hairpin RNA )小发夹RNA
是设计为能够形成发夹结构的非编码小RNA分子,shRNA需通过载体导入细胞后,然后利用细胞内的酶切机制得到siRNA而最终发挥RNA干扰作用。
Ø Dicer:属于RNaseⅢ 家族,是dsRNA的特异性核酸内切酶
Ø RISC:(RNA-inducing silencing complex) RNA诱导的沉默复合体,具有核酸内切、外切以及解旋酶活性
基本概念:
Ø RNAi:(RNA interference)RNA干扰
内源性或外源性双链RNA(dsRNA)介导的能诱导细胞内与其序列同源的特异基因表达沉默或抑制的效应,诱使细胞表现出特定基因缺失的表型,称为RNA干扰,它也是体内抵御外在感染的一种重要保护机制。
Ø siRNA :(small interfering RNAs)小干扰RNA
由长dsRNA裂解而成的一种19-25nt的短片断双链RNA分子,能够以同源互补序列的RNA为靶目标降解特定的mRNA, RNAi的关键效应分子。
Ø shRNAs:(small hairpin RNA )小发夹RNA
是设计为能够形成发夹结构的非编码小RNA分子,shRNA需通过载体导入细胞后,然后利用细胞内的酶切机制得到siRNA而最终发挥RNA干扰作用。
Ø Dicer:属于RNaseⅢ 家族,是dsRNA的特异性核酸内切酶
Ø RISC:(RNA-inducing silencing complex) RNA诱导的沉默复合体,具有核酸内切、外切以及解旋酶活性
二、机制
目前普遍认为,共抑制、基因压制和RNAi很可能具有相同的分子机制,都是通过dsRNA的介导而特异地降解靶mRNA, 抑制相应基因的表达。 即RNAi、共抑制、quelling均属于PTGS!现已初步阐明dsRNA介导的同源性靶mRNA降解过程主要分为两步。
第一步(起始阶段)是较长ds RNA在ATP参与下被RNaseⅢ样的特异核酸酶切割加工成21~23nt的由正义和反义链组成的小干扰RNA(small interfering RNA,siRNA)。
第二步(效应阶段)是siRNA 在ATP参与下被RNA解旋酶解旋成单链,并由其中反义链指导形成RNA诱导的沉默复合体(RNA-induced silencing complex,RISC)。


RNAi途径主要存在于细胞浆中,但是siRNA产生、靶mRNA降解的亚细胞位置尚未明确。外源性(注射或喂养)的dsRNA和病毒性dsRNA可能可以直接进入细胞浆中的RNAi途径,仅在细胞浆中复制的RNA病毒可被dsRNA介导的沉默机制所抑制。外源性dsRNA则还可导致细胞核中的同源早期 RNA转录产物减少。
在许多机体中反向重复转基因序列在细胞核内转录成发夹dsRNA,进而可介导RNAi,这种dsRNA可能需要转移至胞浆中才可有效地沉默同源靶mRNA。
RNAi的放大效应机制
siRNA不仅可引导RISC切割靶RNA,而且可作为引物在RNA依赖的RNA聚合酶(RdRP)作用下以靶mRNA为模板合成新的dsRNA。
新合成的长链dsRNA同样可被RNaseⅢ样核酸酶切割、降解而生成大量的次级siRNA。次级siRNA又可进入合成-切割的循环过程,进一步放大RNAi作用。这种合成-切割的循环过程称为随机降解性PCR(random degradative PCR)。
-
企业风采

-
项目成果
-
企业风采

-
科技前沿

-
科技前沿
-
科技前沿

-
科技前沿

-
并购