杜氏新药Puldysa在欧盟进入审查,有效延缓呼吸功能下降

Santhera Pharmaceuticals是一家专注于开发和商业化创新疗法治疗罕见病和其他疾病的瑞士制药公司。近日,该公司宣布,欧洲药品管理局(EMA)已受理Puldysa(idebenone)的上市许可申请(MMA),该药用于未使用糖皮质激素的杜氏肌营养不良症(DMD)患者治疗呼吸功能障碍。EMA人用医药产品委员会(CHMP)对该MAA的审查程序已经启动,预计2020年中期发表审查意见。
Santhera公司首席医疗官兼开发负责人Kristina Sjoblom Nygren博士表示:“CHMP启动MAA审查是我们取得的一个重要里程碑,目前DMD患者还没有可用的呼吸功能保护疗法。我们期待着在审查过程中与CHMP密切合作,尽快为患者提供Puldysa。”
idebenone是一种合成的短链苯醌(short-chain benzoquinone),这是NAD(P)H:醌氧化还原酶(NQO1)的辅助因子。idebenone能够刺激线粒体电子传递,减少和清除活性氧(ROS)并补充细胞能量水平。在美国和欧盟,idebenone已被授予孤儿药资格,在美国还被授予了快速通道资格。
DMD是一种最常见、最具破坏性的进行性肌肉无力疾病类型,患者从年幼时就开始发生肌肉退化,导致早期发病和呼吸衰竭死亡。DMD是一种遗传性、退行性疾病,由编码抗肌萎缩蛋白(dystrophin,Dys)的基因出现突变导致,该病几乎只发生在男性身上,在全球范围内,活产儿中发病率高达1/3500。DMD的特点是Dys的缺失,导致细胞损伤、钙稳态受损、氧化应激水平升高和肌肉细胞能量生成减少。随着年龄的增长,渐进性的呼吸肌肉无力影响胸副肌和膈肌,导致呼吸系统疾病、气道分泌物清除障碍、无效咳嗽引起的复发性肺部感染,最终导致呼吸衰竭。目前尚无药物获批用于延缓DMD患者呼吸功能的丧失。

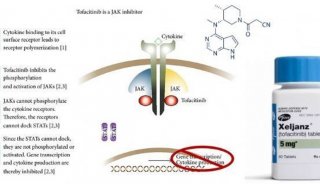
idebenone作用机制(图片来源:Santhera公司网站)
Puldysa MAA的提交,是基于多项II期和III期临床研究的数据,包括一项双盲、安慰剂对照、关键性III期研究DELOS,该研究在64例未接受糖皮质激素治疗的DMD患者中开展,研究中患者接受idebenone(900mg/天)或安慰剂。结果显示,该研究达到了主要终点:治疗52周后,与安慰剂组相比,idebenone治疗组呼气峰值流量(PEF)下降的速度显著降低,表明该药能够减缓患者呼吸功能下降的进程。来自双盲、安慰剂对照II期研究DELPHI及其2年开放标签扩展研究DELPHI-E也为idebenone的疗效提供了支持性数据。
此外,一项前瞻性、回顾性研究SYROS对18例已完成DELOS研究并进入扩大获取项目(EAP)接受idebenone(900mg/天)治疗的患者进行了长期呼吸功能数据的收集和分析。结果显示,在治疗过程中,先前观察到的idebenone对降低呼吸功能下降率的有益作用可维持长达6年。(生物谷Bioon.com)
原文出处:EMA Validates Santhera's Marketing Authorization Application for Puldysa in Duchenne Muscular Dystrophy
-
焦点事件

-
政策法规

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
焦点事件

-
焦点事件

-
政策法规

-
科技前沿
-
科技前沿

-
技术原理

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果

-
项目成果

-
产品技术

-
科技前沿
-
焦点事件

-
项目成果

-
焦点事件

-
焦点事件

-
焦点事件

-
项目成果
-
焦点事件

-
项目成果
-
科技前沿

-
焦点事件