肿瘤标志物的化学发光定量检测
使用化学发光定量检测“肿瘤标志物”时,由于仪器、试剂不同,定量结果存在差异,于是临床医生就认为检测结果不准确。两者之前是否存在可比性?各实验室是否自己制定参考范围,以解释最后结果的正常或异常?
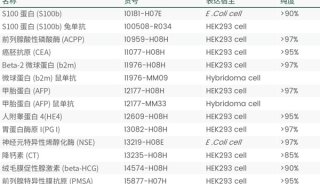
吴健民教授引用了《常用血清肿瘤标志物临床应用指南》一文,文中指出肿瘤标志物检测的方法很多,包括放射免疫测定法,酶联免疫测定法,化学发光免疫测定法,电化学发光免疫测定法,蛋白芯片法等。不同的方法、不同的仪器、不同的试剂,会得出不同的结果,这给临床医生诊断和疗效观察带来困难。
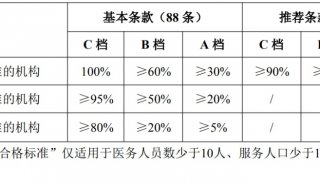
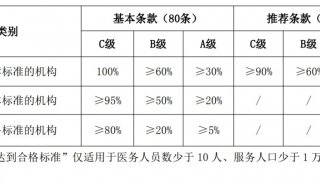
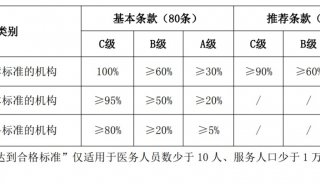
在卫生部临床检验中心公布的肿瘤标志物年度质量控制汇总报告中也可以看到,肿瘤标志物的质控数据离散度很大。为了使各地上报的质控数据可以较好地统计和分析,卫生部临床检验中心将质控数据分为放免组,酶免组,罗氏组,雅培组,西门子组,贝克曼组,安图组,科美生物组,新产业组,上海数康组等分别进行统计,使质控数据相对比较集中。即使这样CA系列的肿瘤标志物其变异系数还是比较大。究其原因,缺乏国际标准品是重要的因素。目前国际标准品仅有AFP,CEA,PSA和hCG等四种,而CA系列的肿瘤标志物还没有国际标准品,因此不同医院,不同仪器的检测结果差异较大,难以互认,也无可比性。在《常用血清肿瘤标志物临床应用指南》一文中指出,在肿瘤标志物连续检测、判断疗效或复发监测时,应使用同一检测系统进行,以保证测定结果的可比性。实验室应尽量避免更换肿瘤标志物的检测方法,如果有方法改变,需告知临床医生并予以说明。
关于肿瘤标志物参考范围,在不同地区、不同人群、不同方法、不同试剂、不同设备测定的情况下,肯定会有一些差别,只是差别的大小而已。现在国内使用的肿瘤标志物检测参考范围基本上是国外的。我们许多实验室是在用外国人制造的仪器和试剂对中国人进行检测,用外国人的参考值来衡量中国人的检测结果是否正常,这本身就不够科学。各实验室宜建立自己的参考范围或对现在使用的参考值进行验证,以适合本地区、本医院的临床实践。
-
焦点事件

-
产品技术

-
焦点事件
-
焦点事件

-
科技前沿

-
项目成果
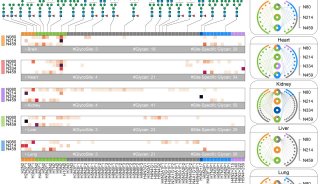
-
综述

-
科技前沿

-
财报

-
科技前沿
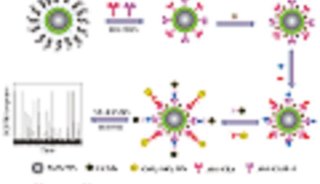
-
科技前沿

-
焦点事件

-
焦点事件

-
科技前沿
-
科技前沿
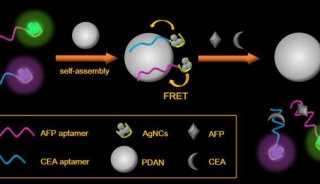
-
产品技术

-
政策法规

-
焦点事件

-
项目成果