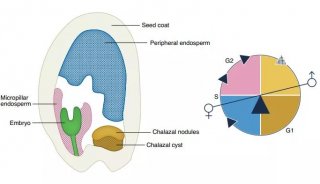
北大邓宏魁《Cell Research》干细胞研究新进展
2014年9月5日,北京大学、军事医学科学院、华大基因、中日友好医院等处的研究人员在国际学术期刊《Cell Research》以“Systematically labeling developmental stage-specific genes for the study of pancreatic β-cell differentiation from human embryonic stem cells”为题发表了一项最新研究成果,在这项研究中,研究人员开发出一种系统的策略,利用hPSCs到胰腺β细胞的直接分化作为模型,通过标记时序发育基因以包含主要的发育阶段,来研究hPSC分化。这种平台和新的研究结果,将为在体外从hESCs获得成熟的β细胞,铺平道路。
本研究通讯作者分别为北京大学生科院的邓宏魁教授和工学院的席建忠教授。本研究受到国家重点基础研究发展项目(973项目)、关键新药创新和制造项目、科技部、国家自然科学基金、教育部和国家科技重大专项支撑项目(深圳)的资助支持。
人类多能干细胞(hPSCs),包括人类胚胎干细胞(hESCs)和诱导多能干细胞,可以通过循序渐进地模仿关键的发育事件,被有效地诱导成不同类型的细胞,从而有巨大的潜力用于研究发育生物学、疾病模型和细胞替代疗法。尽管在过去的十年中,研究人员已经付出了很大的努力,但是还没有在体外获得完全成熟的细胞类型,这大大阻碍了这些hPSC衍生细胞的进一步应用。为了在体外能够从hPSCs获得成熟的细胞类型,有两个主要的问题仍然需要解决。
首先,因为目前用于hPSC分化的最好程序,通常是以一种循序渐进的方式进行的,所以,每一个阶段(尤其是早期阶段)诱导过程中的偏差,都将会积累并可能被逐步显著放大。以前对于hPSCs定向分化为胰腺β细胞的研究表明,胰岛素(INS)生产细胞在后期的产量,对于最初两个阶段的TGF-β信号的强度和时间都很敏感。此外,每一步产生的细胞实际上是异质的。意外的细胞-细胞间相互作用和多余细胞所分泌的因子,将会掩盖所需的信号,并误导分化过程。因此,为了优化诱导条件,并由此为整个逐步分化过程的精确控制做好准备,制定某种策略让我们可以监测整个分化过程的动力学和纯化理想的细胞群,将具有很大的帮助。
第二,当前hPSC分化程序的建立,在很大程度上依赖于发育学知识,主要从非人类实验模型(特别是小鼠)推论得出。在胰腺的情况中,两个物种对于胰腺发育过程中关键调节因子(如GATA6)的需求有所不同,表明发育机制可能存在较大差异。此外,即使在小鼠模型中,胰腺β细胞的发育过程还存在一些知识差距,导致缺乏定向分化的足够发育线索。因此,很有必要开发适当的工具,让体外衍生的细胞群在每个阶段进行分离,以进行仔细评估,从而揭示发育的不太为人了解的方面。
总的来说,为了解决上述问题,如果有一种系统策略可监测、纯化和分析每一阶段的hPSC衍生中间细胞,将是非常可取的。此前有研究表明,遗传标记,尤其是谱系特异性转录因子,可以用于hPSCs发育和分化的研究。然而,一定程度上因为传统基因打靶技术的效率较低,这类研究主要集中在分化过程,不能为整个连续过程的研究提供一种系统的解决方案。近年来,基因打靶策略所取得的突破,使我们能够高效地进行某些细胞谱系的系统基因标记。
在这项研究中,研究人员借助于转录激活因子样效应物核酸酶(TALEN),系统地标记了胰腺发育过程中的次序基因,首次覆盖了来自hESCs的胰腺β细胞的主要发育阶段。因而产生了一大组报告细胞系(reporter cell lines);其中几个细胞是在NGN3-eGFP细胞系基础上建立的双报告细胞系。利用这种独特的平台,研究人员成功地实时可视化整个分化过程的动力学,使我们能够识别并因此分离每个分化阶段的中间细胞群,用于进一步分析。
研究人员使用双报告hESC细胞系,捕获了细胞命运转变的过程,揭开了多个细胞亚群的基因表达谱。研究通过RNA测序,进一步分析了hPSC衍生的NGN3-eGFP+细胞,并将sushi domain-containing 2(SUSD2)确定为一种新型的表面蛋白,在hESC衍生的胰细胞和发育的人胰腺中,胰腺内分泌祖细胞和早期内分泌细胞都富含这种蛋白。这个平台和这些新的研究结果,将为体外从hESCs获得成熟的β细胞,铺平道路。
-
项目成果

-
焦点事件
-
焦点事件

-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿

-
技术原理

-
项目成果

-
项目成果

-
项目成果
-
科技前沿
-
焦点事件

-
焦点事件

-
项目成果
-
项目成果
-
项目成果
-
科技前沿
-
焦点事件
-
科技前沿