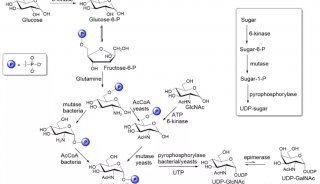
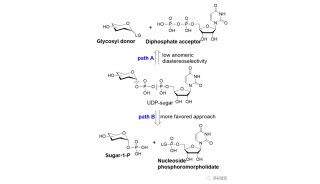
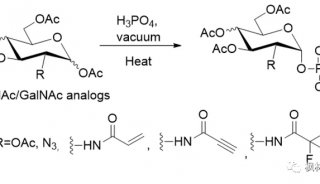
毛细管电色谱及其在药物分析中的应用(一)
毛细管电色谱[1~3](Capillary Electrochromatography,CEC)是近10年来综合了现代最新分离技术高效液相色谱(High Performance Liquid Chromatography,HPLC)和毛细管电泳(Capillary Electrophoresis,CE)的优势而发展起来的高效电分离微柱液相色谱技术。CEC一般采用熔融石英毛细管,在柱内填充或在柱壁键合固定相,用高压直流电源(或加一定的压力)代替高压泵,即用电渗流(Electroosmotic Flow,EOF)驱动流动相,溶质依据它们在流动相与固定相中的分配系数的不同和自身电泳淌度的差异得到分离,既能分离中性物质又能分析带电组分。因此,可将它定义为“一种溶质与固定相间的相互作用占主导地位的电泳过程”。CEC是HPLC和CE的有机结合,不仅具有CE水平的高柱效,同时还具有HPLC的选择性。它克服了CE选择性差和分离中性物质的困难,同时大大提高了液相色谱的分离效率,开辟了高效微分离技术的新途径。近年来,随着CEC柱制备技术、分离机制、仪器设备的不断研究和发展,CEC已在分析领域中引起广泛关注,并在有机小分子分离、环境分析、药物分析和生化分析等方面得到应用。本文就CEC的基本原理、研究进展及其在药物分析中的应用作一概述。
1 发展概况
1974年,Pretorius等[4]首先在薄层色谱和液相色谱中应用EOF驱动机制,但并未引起广泛的注意。1981年,Jorgenson等[5]在170 μm内径的毛细管中填充10 μm的ODS固定相,以EOF推动流动相,对中性化合物进行分离,获得31000.m-1理论塔板数的柱效,在此模式下填料的不规则度对区带展宽并不重要。尽管在当时具体实施和操作有相当困难,但作者认为利用EOF进行液相色谱是可行的。1982年,Tsuda等[6]在毛细管壁键合固定相,首次实现电驱动开管液相色谱,即开管电色谱(OT-CEC),1987年Knox 等[7]用拉伸方法在50 μm内径毛细管中填充5 μm颗料,获得69000.m-1的理论塔板数,并证明了在EOF驱动体系中,可使用更细粒度填料。他们的理论和实验都表明CEC在柱效上明显优于HPLC。
进入90年代,随着CE的全面开展和电色谱柱制备技术的提高,CEC迅速位于分析化学的前沿,因为它集CE和HPLC的优势于一身,无论从柱效、选择性,还是分析速度上,都达到或超过现有的电泳和色谱方法。1992年,Yamamoto等[8]观察到在不降低柱效的前提下,线性EOF速度可增加到3 mm.s-1,保留时间的重现性良好,相对标准差小于2 %。1994年,Smith等[9]进行电色谱分析,在加压下减少气泡形成,柱效为380000.m-1理论塔板数。1995年,Yan等[10]在150 μm内径毛细管中填充90 %的3 μm ODS和10 %的1 μm硅胶颗粒,通过激光诱导荧光检测,获得400000.m-1理论塔板数的柱效;Smith等[11]用离子交换固定相在pH<3时分离酸性药物,取得了令人难以置信的8×106.m-1理论塔板数的柱效,展示了非常诱人的前景。近1年来,国内外有关CEC的分离机制、柱制备、应用研究以及全面的综述文章迅速增加[12~36]。并于1997年8月在美国加州召开了第一届毛细管电色谱会议,表明在分析领域中已出现毛细管电色谱这一新的研究热点。
2 基本特性
CEC主要有以下特点:(1)采用的是电场驱动的EOF,EOF扁平的流型较HPLC的抛物线流型有高得多的柱效。(2)没有背压问题,可以使用更小粒度的填料和更长的毛细管柱,具有更高的分辨能力。(3)在高pH下EOF很大,CEC有可能解决大范围中性粒子的分离问题。(4)在分离中性粒子时,CEC不需要像胶束电动色谱(Micellar Electrokinetic Chromatography,MEKC)那样使用表面活性剂,有利于和MS联用。(5)在低pH下,如果选择合适的填料,如离子交换树脂,也可对带电组分达到很好的分离。(6)CEC类似于CE采用在柱检测,检测的死体积很小,有利于提高柱效和检测灵敏度。(7)加压电色谱(PEC)是在加电压的同时,附加一定压力驱动流动相,其优点是避免分离过程中产生气泡,提高稳定性。又可用压力来控制流速,缩短分离时间,并能实现CEC的梯度洗脱[37,38]。(8)目前在HPLC中已使用的分离模式在CEC中均可以实现。
3 分离机制
3.1 保留机理 CEC的保留机理可用下式表示,溶质的迁移速率(uex)为:
(1)
其中
(2)
(3)式中uep和ueo分别为溶质的电泳速度和电渗流,k’为溶质的容量因子,εr和εo分别为相对介电常数和绝对介电常数,ξ和η分别为Zeta电势和流动相的粘度,V、E和L分别为电压、电场强度和色谱柱的总长,q和r分别为溶质的电量和半径。
式(1)表明溶质在柱中的保留是与它在两相中分配常数有关的,因而它是一种色谱行为。但当分析物是离子时,其保留机制又类似于CE,根据其电泳淌度和分配系数的不同得以分离。因而,CEC在选择性和使用范围上兼顾了CE和HPLC的优点。
3.2 柱效 类似于HPLC,CEC的柱效可用Van Deemter方程表征:(4)
式中A项为涡流扩散项,代表在填充床中由于流速的不同而引起的谱带展宽,在EOF推动下,只要毛细管的内径大于20倍的双电层厚度,管中的流速几乎是不随柱径和填料的大小改变的,而双电层的厚度一般为10 nm,所以A项对塔板高度的贡献可以不计。C项为传质阻力项,主要是由溶质在填充微粒内部的扩散系数(Dsz)所决定,Yamamoto等[8]的研究表明在一般操作条件下,C项对塔板高度的贡献也是很小的。那么,在CEC中决定塔板高度的主要是B项,即纵向扩散项。因此,在柱效上CEC远优于HPLC。
3.3 影响分离的因素
3.3.1 电压 在柱长一定的情况下,增大电压则加大EOF,有助于柱效的提高,但电压过高时会导致气泡产生而造成EOF消失。
3.3.2 有机溶剂 向缓冲液中加入乙腈后,溶液的粘度减小,一般随有机溶剂浓度增大,电渗流增加。但是,在流动相中采用不同的溶剂对EOF会产生不同的影响。
3.3.3 pH EOF随流动相的pH增大而加大。这是因为当pH增大时,毛细管壁上硅醇基电离度增大,Zeta电势增大。因此,可利用高pH达到快速分离。
3.3.4 电解质 随电解质浓度增大,EOF的线速度会因Zeta电势的减小而下降。在提高电解质浓度时,要考虑焦耳热问题。当缓冲溶液中电解质浓度在1~10 m mol.L-1范围内焦耳热的影响较小。Boughtflower等[39]报道了使用两性电解质缓冲溶液,如Tris等,可以在更高浓度(100 m mol.L-1)下操作。
3.3.5 填料粒度 在填料粒度大于1 μm情况下,EOF的速度和流型不会随粒度的减小而改变,故可以采用小颗粒来提高柱效。
-
科技前沿

-
综述

-
企业风采

-
精英视角

-
技术原理

-
产品技术

-
科技前沿

-
综述
-
综述
-
会议会展

-
科技前沿
-
项目成果
-
科技前沿
-
综述

-
综述
-
技术原理
-
焦点事件

-
技术原理

-
焦点事件

-
焦点事件

-
焦点事件

-
综述
-
综述