华人学者PNAS发表CRISPR新技术
复杂的生物学现象受到不同基因的协调控制。在人类细胞中系统地鉴定这些基因组合是非常麻烦的,亟需一种可扩展的多重筛选技术。
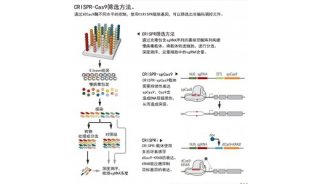
美国麻省理工的研究人员最近在美国国家科学院院刊PNAS杂志上发布了多重条码的CRISPR-Cas9筛选平台。该平台结合了CRISPR-Cas9和CombiGEM技术,能够在人类细胞中对带条码的基因扰动组合进行大规模平行筛选。
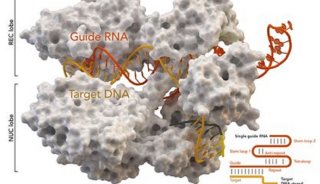
CRISPR-Cas9原本是细菌在漫长的进化史中演化出的重要防御机制。规律成簇的间隔短回文重复CRISPR与内切酶Cas9的组合,可以在引导RNA的指引下,靶标并切割入侵者的遗传物质。 CRISPR-Cas系统不仅操作简便,还有着很强的可扩展性,快速渗透到了生物学研究的各个领域。
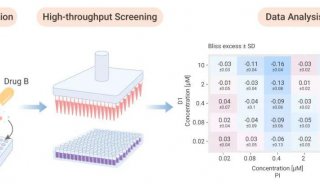
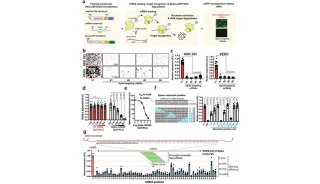
研究人员用CombiGEM-CRISPR建立了筛选文库,包括23,409个带条码的双引导RNA(gRNA)组合。他们由此鉴定了能够抑制卵巢癌细胞生长的gRNA组合以及相应的基因对,并通过CRISPR-Cas基因敲除和RNAi基因敲低进行了验证。研究人员还测试了靶标这些基因对的小分子组合,发现它们的确能对卵巢癌细胞起到协同的抗增殖效果。
研究人员认为CombiGEM-CRISPR平台有着广泛的应用前进,有助于快速鉴定调节人类疾病表型的基因组合,并将其转化为有效的药物组合。领导这项研究的卢冠达(Timothy Lu)博士是MIT生物工程、电子工程及计算机科学系的副教授,这位青年科学家曾被麻省理工的百年期刊《技术评论》评为世界青年科技创新家。
近来,卢冠达博士陆续发表了多项CRISPR研究成果。他的研究团队利用CRISPR-Cas9成功靶标了那些让细菌耐受抗生素的基因。这项发表在Nature Biotechnology杂志上的研究显示,CRISPR-Cas9可以让细菌的耐药基因和致病基因丧失功能,帮助人们选择性杀死危害比较大的致病菌。
卢冠达博士还在Molecular Cell杂志上发表文章,介绍了一个以CRISPR-Cas9为基础的基因组靶向技术——CRISPR-Display (CRISP-Disp)。近年来人们逐渐意识到非编码RNA并不是基因组中的垃圾序列,而是许多基础生命过程的核心。许多非编码RNA的具体功能和作用机制目前还鲜为人知。卢冠达博士在文章中详细阐述了CRISP-Disp技术在非编码RNA研究领域的应用前景。
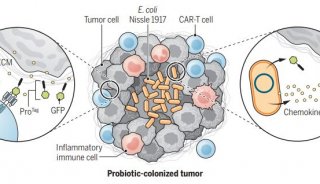
对肠道微生物进行基因工程改造可以实现各种各样的应用,比如调节肠道生态环境和治疗人类疾病。多形拟杆菌是普遍存在于人类肠道微生物组的一种高丰度共生菌,很适合用来进行这类研究。卢冠达博士的研究团队利用CRISPR技术开发了可以改造多形拟杆菌的多种遗传学元件,并在此基础上成功改造了多形拟杆菌,让其能够感知并应答肠道菌群中的刺激。
-
科技前沿

-
项目成果

-
焦点事件

-
焦点事件

-
科技前沿

-
科技前沿

-
市场商机

-
焦点事件

-
焦点事件

-
产品技术
-
焦点事件

-
产品技术
-
产品技术
-
科技前沿
-
综述
-
企业风采

-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿

-
项目成果
-
项目成果
-
焦点事件

-
项目成果
-
科技前沿
-
项目成果
-
科技前沿
-
科技前沿
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿
-
项目成果
-
焦点事件
-
项目成果
-
焦点事件

-
科技前沿
-
焦点事件
-
项目成果
-
项目成果
-
焦点事件

-
项目成果
-
并购

-
科技前沿
-
焦点事件

-
焦点事件

-
技术原理

-
技术原理
-
技术原理
-
项目成果
-
精英视角

-
焦点事件
-
焦点事件
-
焦点事件

-
项目成果
-
科技前沿
-
项目成果
-
焦点事件