HoloMonitor M4应用抗血管生成治疗肿瘤研究
前言
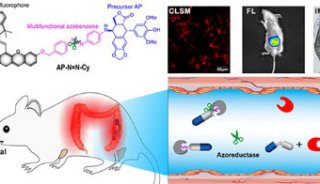
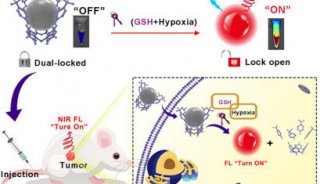
虽然抗血管生成anti-angiogenic (AA)治疗已经广泛应用到了临床的肿瘤治疗中,截至目前,仍然还存在着药效不足和内在抗性的两大问题,有些研究表明抗血管生成治疗甚至有可能增加肿瘤转移可能性。但是,具体是因为抗血管生成的药物作用导致的这种肿瘤转移还是这中治疗方法本身具有一定的“缺陷”。本研究中,我们利用物理障碍的方法完全阻止肿瘤的血液供应,观察肿瘤的运动形态变化。
实验结果
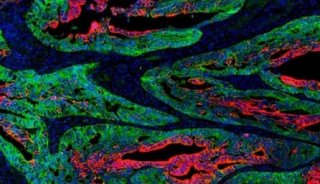
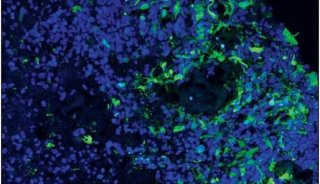
研究前期的实验使用物理屏障的方法去阻碍血液供应,结果显示被切断血液供应的肿瘤细胞没有受到影响反而在其周围又生成新的肿瘤组织,进一步发现原发性肿瘤细胞会发生形变异穿过阻断血液供应的物理屏障,从而侵袭外周组织形成新的肿瘤组织。
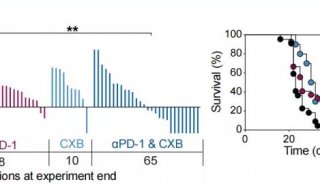
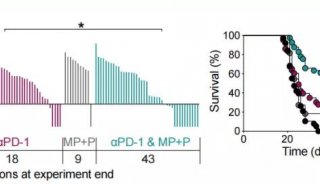
以上前期的实验结果与未阻断血液供应的肿瘤细胞同实验对比发现,两种实验小鼠的死亡率并没有明显的差异,也就是可能这种短期的抗血管新生的治疗方案不能有效的治疗肿瘤,反而有可能会造成更糟糕的结果。
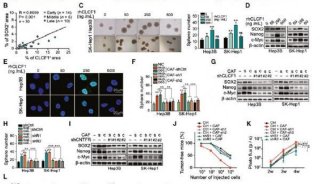
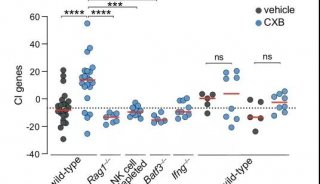
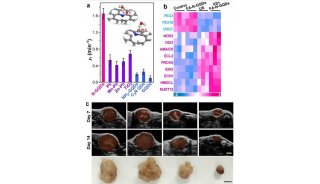
由原发性肿瘤外周区域诱发的二次肿瘤,可能会携带上某些侵袭能力或者是具有抵抗抗血管生成的药物的耐药性,为了确定是否会影响肿瘤的迁移性,分别收集物理阻断肿瘤组织后逃逸细胞、未阻断肿瘤组织迁移细胞、和原发性肿瘤细胞,分别被称之为Escaped cells,Migrated cells,Primary cells, 利用瑞典的激光全息活细胞成像及分析系统(HoloMonitor M4)进行24小时监测,4min拍摄一次,使用Hstudio2.6.1分析19个细胞的迁移运动距离及运动速率等,实验结果显示Escaped cells,Migrated cells,的整体运动性明显大于Primary cells,Escaped cells的运动性大于Migrated cells,Transwell实验结果同时验证这种结果。表明在从阻断肿瘤组织中迁移逃逸出的细胞的运动侵袭性明显增加。

因此,AA治疗创造了一个极端环境的营养和氧气不足,但不能阻止癌症细胞迁移,而导致肿瘤细胞被迫逃离“饥饿”区域侵袭到其他位置,此时,毫无疑问的是原发性肿瘤组织因血液供应不足而萎缩,但是逃逸出来的细胞则会诱发二次肿瘤,甚至扩散全身。因此,即使肿瘤的侵袭性并没有增加,那“血液不足”本身也会引起肿瘤转移。大多数的导致患者死亡的不是原发性肿瘤而是转移性肿瘤,所以AA治疗的好处到底在哪儿?
The “inherent vice” in the anti-angiogenic theory may cause the highly metastatic cancer to spread more aggressively 张巍 ,分子医学研究中心,四川大学华西医院:
-
科技前沿

-
科技前沿
-
焦点事件

-
科技前沿

-
科技前沿

-
焦点事件

-
焦点事件

-
项目成果
-
产品技术

-
科技前沿

-
焦点事件

-
综述
-
焦点事件

-
项目成果

-
精英视角

-
科技前沿
-
科技前沿

-
科技前沿

-
焦点事件

-
项目成果

-
焦点事件

-
焦点事件
-
项目成果
-
技术原理

-
综述
-
会议会展

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件
-
综述
-
项目成果
-
项目成果
-
项目成果
-
科技前沿

-
政策法规